题目内容
13.从海水中可以提取溴,主要反应之一为2Br-+Cl2═2Cl-+Br2,下列有关说法中正确的是( )| A. | 溴离子具有氧化性 | B. | 氯气是还原剂 | ||
| C. | 该反应属于复分解反应 | D. | 氯气氧化性比溴单质强 |
分析 反应2Br-+Cl2=2Cl-+Br2中Cl元素化合价降低,Cl2为氧化剂,Br元素化合价升高,被氧化,Br-为还原剂,以此解答该题.
解答 解:A.溴离子化合价处于最低价态,只具有还原性,故A错误;
B.反应中Cl元素化合价降低,Cl2为氧化剂,故B错误;
C.反应中有元素化合价的升降,为氧化还原反应,故C错误;
D.根据氧化剂氧化性大于氧化产物氧化性,可知氯气的氧化性比溴单质强,故D正确.
故选D.
点评 本题考查氧化还原反应,侧重于基本概念的考查,注意从元素化合价的角度认识氧化还原反应的相关概念和性质,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.将Na、Na2O、Na2O2的混合物4.34g与足量的水反应,在标准状况下得到672mL混合气体,放电条件下,气体之间恰好完全反应,则它们的物质的量之比为( )
| A. | 1:1:1 | B. | 1:2:1 | C. | 1:1:2 | D. | 4:3:2 |
4.已知4个锌原子能与10个硝酸分子反应,生成硝酸锌和硝酸铵及水,则下列说法不正确的是( )
| A. | 该反应中硝酸表现了氧化性和酸性 | |
| B. | 硝酸铵既是氧化产物又是还原产物 | |
| C. | 该反应中被氧化与被还原的物质的质量比为260:63 | |
| D. | 该反应中电子转移数目为8e- |
1. 中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
(1)从图实验装置看,其中尚缺少的一种玻璃用品是环形玻璃搅拌棒,除此之外,装置中的一个明显错误是大烧杯杯口与小烧杯杯口没有相平,两烧杯之间没有塞满碎泡沫塑料.
(2)为保证该实验成功该同学采取了许多措施,如图的碎纸条的作用在于隔热,减少热量的损失.
(3)若改用60mL 0.25mol•L-1 H2SO4和50mL 0.55mol•L-1 NaOH溶液进行反应与上述实验相比,所放出的热量不相等(填“相等”、“不相等”),若实验操作均正确,则所求中和热相等(填“相等”“不相等”)
(4)倒入NaOH溶液的正确操作是:C. (从下列选出).
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(5)使硫酸与NaOH溶液混合均匀的正确操作是:D. (从下列选出).
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用一种特殊的搅拌棒轻轻地搅动
(6)实验数据如表:
①请填写下表中的空白:
②近似认为0.55mol/L NaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=-56.8kJ•mol-1( 取小数点后一位).
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)abc.
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中.
 中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:(1)从图实验装置看,其中尚缺少的一种玻璃用品是环形玻璃搅拌棒,除此之外,装置中的一个明显错误是大烧杯杯口与小烧杯杯口没有相平,两烧杯之间没有塞满碎泡沫塑料.
(2)为保证该实验成功该同学采取了许多措施,如图的碎纸条的作用在于隔热,减少热量的损失.
(3)若改用60mL 0.25mol•L-1 H2SO4和50mL 0.55mol•L-1 NaOH溶液进行反应与上述实验相比,所放出的热量不相等(填“相等”、“不相等”),若实验操作均正确,则所求中和热相等(填“相等”“不相等”)
(4)倒入NaOH溶液的正确操作是:C. (从下列选出).
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(5)使硫酸与NaOH溶液混合均匀的正确操作是:D. (从下列选出).
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用一种特殊的搅拌棒轻轻地搅动
(6)实验数据如表:
①请填写下表中的空白:
| 温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差 平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | 3.4℃ |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)abc.
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中.
8.某饱和一元醇与浓硫酸共热得到一种无同分异构体的烯烃,该醇分子中的碳原子数一定为( )
| A. | 1 | B. | 4 | C. | 3 | D. | 6 |
18.将含0.4mol•L-1Cu(NO3)2和0.4mol•L-1KCl的水溶液500mL,用惰性电极电解一段时间后,在一个电极上析出0.15mol Cu,此时在另一电极上放出气体,在标准状况下约为( )
| A. | 5.6L | B. | 6.72L | C. | 8.4L | D. | 2.8L |
2.下列所描述的变化不属于化学变化的是( )
| A. | 用一种原子制造出另一种或几种原子 | |
| B. | 碳酸氢铵受热分解 | |
| C. | 蓝矾加热后变为白色固体 | |
| D. | 电解水生成氢气和氧气 |
3.下列溶液存在的是( )
| A. | c(Na+)=1mol/L,c(Cl-)=1mol/L,c(Ca2+)=2mol/L,c(ClO4-)=4mol/L | |
| B. | c(K+)=1mol/L,c(Mg2+)=1mol/L,c(Cu2+)=1mol/L,c(NO${\;}_{3}^{-}$)=4mol/L | |
| C. | c(OH-)=1mol/L,c(SO${\;}_{4}^{2-}$)=1mol/L,c(NH${\;}_{4}^{+}$)=6mol/L,c(HCO${\;}_{3}^{-}$)=1mol/L | |
| D. | c(Al3+)=1mol/L,c(SO${\;}_{4}^{2-}$)=1mol/L,c(OH-)=2mol/L,c(Na+)=2mol/L |
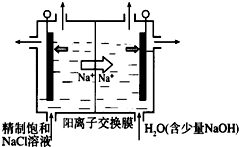 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.