题目内容
下列反应的离子方程式书写正确的是( )
①硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-=BaSO4 ↓
②将金属钠加入水中2Na+2H2O=2Na+ +2OH-+H2↑
③石灰石溶于稀醋酸:CaCO3+2CH3COO H=2CH3COO- +Ca2+ +CO2↑+H2O
④氯气与水反应:Cl2+H2O H++Cl-+HClO
H++Cl-+HClO
⑤小苏打溶液中加入少量石灰水:Ca2++ 2OH-+2HCO3-=CaCO3↓+CO32-+2H2O
⑥次氯酸钙溶液中通入过量CO2:Ca2++2C1O-+CO2+H2O=CaCO3↓+2HC1O
⑦钠与硫酸铜溶液反应:Cu2+ +2Na=Cu+2Na+
⑧纯碱溶液中滴加少量盐酸:CO32-+H+=HCO3-
A.①②⑤ B.②③④⑤⑧ C.④⑤⑥⑦ D.②③⑧
 备战中考寒假系列答案
备战中考寒假系列答案某小组同学在实验室里对Fe3+与I﹣的反应进行探究,实现Fe3+与Fe2+相互转化.
(1)甲同学首先进行了如下实验:
编号 | 操作 | 现象 |
Ⅰ | 先向2mL0.1mol•L﹣1FeCl2溶液中滴加KSCN溶液,再滴加新制氯水 | ___________________ ___________________ |
Ⅱ | 先向2mL0.1mol•L﹣1FeCl3溶液中滴加KSCN溶液,再滴加0.1mol•L﹣1KI溶液 | 滴加KSCN溶液后,溶液变成血红色;滴加0.1mol•L﹣1KI溶液后,血红色无明显变化 |
实验Ⅰ中发生反应的离子方程式为 , .
(2)实验II的现象与预测不同,为探究可能的原因,甲同学又进行了如下实验,
操作及现象如下:
编号 | 操作 | 现象 |
Ⅲ | 向2mL0.1mol•L﹣1KI溶液中滴加1mL 0.1mol•L﹣1FeCl3溶液,再滴加KSCN溶液 | 滴加FeCl3溶液后,溶液变成黄色;滴加KSCN溶液后,溶液变成血红色 |
根据实验Ⅲ,该同学认为Fe3+有可能与I﹣发生氧化还原反应.请结合实验现象说明得出该结论的理由: .
(3)乙同学认为,还需要进一步设计实验才可证明根据实验Ⅲ中现象得出的结论.
请补全下表中的实验方案:
编号 | 操作 | 预期现象及结论 |
Ⅳ | 向2mL0.1mol•L﹣1KI溶液中滴加1mL 0.1mol•L﹣1 FeCl3,溶液变黄色,取该溶液于两支试管中, 试管①中滴加 , 试管②中滴加 . | 预期现象① , ② . 结论 . |
(4)上述实验结果表明,Fe3+有可能与I﹣发生氧化还原反应.进一步查阅资料知,参加反应的Fe3+和I﹣物质的量相同.该小组同学结合上述实验结论,分析了实验Ⅲ中加入KSCN后溶液变血红色的原因,认为Fe3+与I﹣反应的离子方程式应写为: .


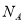
 的混合物中含有的碳原子数目为3NA
的混合物中含有的碳原子数目为3NA