题目内容
某温度下,向密闭容器中加入1 mol N2和3 mol H2,使之反应合成NH3,达到平衡后测得NH3的体积分数为m%;若T不变,只改变起始加入量,使反应达到平衡后,NH3的体积分数仍为m%。若N2、H2、NH3的加入量分别用x、y、z表示,应满足:(1)恒温(T)、恒容(V)条件下:
①若x=0,y=0,则z=_________。
②若x=0.75 mol,则y=_________,z=_________。
③x、y、z应满足的一般关系条件是_________。
(2)恒温(T)、恒压(p)条件下:
①若x=0,y=0,则z_________。
②若x=0.75 mol,则y=_________,z_________。
③x、y、z应满足的一般关系条件是_________。
解析:(1)恒温、恒容条件下的等效平衡:等效配比经“等价转换”成同一边的物质后,各物质的物质的量对应相等。
N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
原始配比: 1 3 0
等效配比: 0 0 z
即: 0.5z 1.5z 0
![]()
即:z=2 mol
N2(g) + 3H2(g)![]() 2NH3(g)
2NH3(g)
等效配比② 0.75 y z
即: 0.75+0.5z y+1.5z 0
则![]()
即:y=2.25 mol z=0.5 mol
N2(g) + 3H2(g)![]() 2NH3(g)
2NH3(g)
等效配比③ x y z
即: x+0.5z y+1.5z 0
则![]()
(2)恒温、恒压条件下的等效平衡:等效配比经“等价转换”成同一边的物质后,各物质的物质的量对应的比例。
N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
原始配比: 1 3 0
等效配比① 0 0 z
即: 0.5z 1.5z z
则![]()
即:z>0,
故z为任意大于零的数。
同理可分析等效配比②和③。
答案:(1)①2 mol ②2.25 mol 0.5 mol ③x+0.5z=1,y+1.5z=3 (2)①>0 ②2.25 mol ≥0 ③y=3x,z≥0(但x、y、z不能同时为0)

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 4C(l)+2D(g).平衡时测得n(C)=1.6mol.下列说法正确的是( )
4C(l)+2D(g).平衡时测得n(C)=1.6mol.下列说法正确的是( )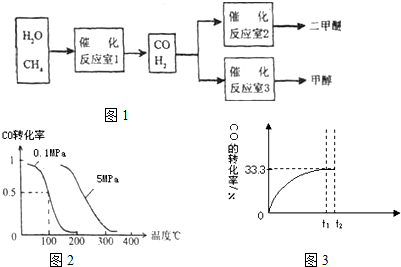
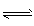 2CO2(g)+4H2O(g),试写出该条件下反应的平衡常数(K)___________ ; 在电脑的使用过程中,电池的温度往往因为各种原因会升高,试判断温度升高时该反应的平衡常数(K)____________(填增大、减小、不变),其反应的正反应速率 ___________(填增大、减小、不变);温度升高_________(填有利或不利于)电池将化学能转化为电能。
2CO2(g)+4H2O(g),试写出该条件下反应的平衡常数(K)___________ ; 在电脑的使用过程中,电池的温度往往因为各种原因会升高,试判断温度升高时该反应的平衡常数(K)____________(填增大、减小、不变),其反应的正反应速率 ___________(填增大、减小、不变);温度升高_________(填有利或不利于)电池将化学能转化为电能。 
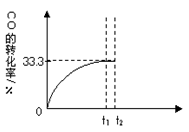
 CO2(g)+H2(g)。 CO的转化率随时间变化关系如图,回答下列问题:
CO2(g)+H2(g)。 CO的转化率随时间变化关系如图,回答下列问题: