题目内容
下列溶液中c(Cl-)与100mL 0.1mol?L-1AlCl3溶液中c(Cl-)相等的是( )
| A、100 mL0.1 mol?L-1的NaCl溶液 |
| B、50 mL 0.2 mol?L-1KCl溶液 |
| C、150 mL 0.15 mol?L-1的MgCl2溶液 |
| D、20 mL 0.5 mol?L-1FeCl3溶液 |
考点:物质的量浓度的相关计算
专题:
分析:离子的物质的量浓度=溶质的物质的量浓度×一个溶质分子中含有的离子的个数,与溶液的体积无关,如:0.1mol?L-1AlCl3溶液中c(Cl-)=0.1mol/L×3=0.3mol/L,据此进行解答.
解答:
解:100mL 0.1mol?L-1AlCl3溶液中Cl-的物质的量浓度为:0.1mol/L×3=0.3mol/L,
A、100ml 0.1mol/L的NaCl溶液所含Cl-物质的量浓度为:0.1mol/L×1=0.1mol/L,故A错误;
B、50mL0.2 mol?L-1KCl溶液中,氯离子浓度为:0.2mol/L×1=0.2mol/L,故B错误;
C、150 mL 0.15 mol?L-1的MgCl2溶液中,氯离子浓度为:0.15mol/L×2=0.3mol/L,故C正确;
D、20mL 0.5 mol?L-1FeCl3溶液中,氯离子浓度为:0.5mol/L×3=1.5mol/L,故D错误;
故选C.
A、100ml 0.1mol/L的NaCl溶液所含Cl-物质的量浓度为:0.1mol/L×1=0.1mol/L,故A错误;
B、50mL0.2 mol?L-1KCl溶液中,氯离子浓度为:0.2mol/L×1=0.2mol/L,故B错误;
C、150 mL 0.15 mol?L-1的MgCl2溶液中,氯离子浓度为:0.15mol/L×2=0.3mol/L,故C正确;
D、20mL 0.5 mol?L-1FeCl3溶液中,氯离子浓度为:0.5mol/L×3=1.5mol/L,故D错误;
故选C.
点评:本题考查物质的量浓度的计算,题目难度不大,注意离子浓度与溶质的浓度的关系即可解答,注意明确离子浓度与溶液体积大小无关.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
下列实验方案正确且能达到相应实验预期目的是( )
A、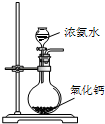 制备少量氨气 |
B、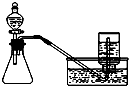 用铜和浓硝酸制取少量NO2 |
C、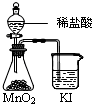 比较MnO2、Cl2、I2的氧化性 |
D、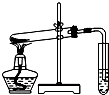 探究NaHCO3的热稳定性 |
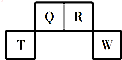
短周期四种元素离子W2+、X-、Y2-、Z+的电子层结构相同.下列说法正确的是( )
| A、原子序数:W>Z>X>Y |
| B、离子半径:r(W2+)>r(X-)>r(Y2-)>r(Z+) |
| C、Y的气态氢化物比X的气态氢化物稳定 |
| D、氢氧化物碱性强弱:W(OH)2>ZOH |
下列各组离子在溶液中不能大量共存的是( )
| A、H2PO4-、NH4+、K+、Mg2+ |
| B、Mg2+、Na+、Cl-、F- |
| C、H+、Cl-、SO42-、K+ |
| D、K+、Zn2+、Br-、NO3- |
下列有关物质的说法正确的是( )
| A、玻璃、陶瓷、水泥、光导纤维的化学组成都是硅酸盐 |
| B、液氨汽化时要吸收大量的热,可用作制冷剂 |
| C、二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 |
| D、生石灰能与水反应,可用来干燥氯气 |
化学与生产、生活、社会密切相关.下列有关说法中正确的是( )
| A、顺丁橡胶、腈纶、涤纶和“人造棉花”都属于合成纤维 |
| B、天宫一号使用的碳纤维是一种新型有机高分子材料 |
| C、绿色荧光蛋白质(GFP)是高分子化合物,不可降解,其水溶液有丁达尔效应 |
| D、“玉兔”月球车太阳能电池帆板的材料是晶体硅 |
分子式为C8H10的某有机物,它能使酸性高锰酸钾溶液褪色,但不能与溴水反应,该化合物在一定条件下与H2完全加成,加成后产物的一氯代物的同分异构体有( )
| A、17种 | B、18种 |
| C、19种 | D、20种 |