题目内容
9.最近科学家用巨型计算机进行模拟后确认,由60个N原子可结合成N60分子,N60变成N2时放出巨大能量.下列有关N60的说法不正确的是( )| A. | N60与N2是同素异形体 | B. | N60一定是比N2更稳定的分子 | ||
| C. | N60的相对分子质量为840 | D. | N60可能是一种很好的火箭燃料 |
分析 A.同素异形体是指由同种元素组成的不同单质;
B.能量越低越稳定;
C.根据相对原子质量计算;
D.火箭燃料在发生反应时要放出巨大的能量来推动火箭运行.
解答 解:A.N60与N2是同种元素组成的不同单质,属同素异形体,故A正确;
B.N60变成N2时放出巨大能量,说明N2比N60能量低,更稳定,故B错误;
C.N60的相对分子质量为14×60=840,故C正确;
D.火箭燃料在发生反应时要放出巨大的能量来推动火箭运行,已知N60变成N2时放出巨大能量,所以N60可能是一种很好的火箭燃料,故D正确.
故选B.
点评 本题考查同素异形体、化学变化、放热反应等,难度较小,旨在考查学生对基础知识的识记,注意基础知识的积累掌握

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
20.下列有机物检验方法正确的是( )
| A. | 用燃烧的方法鉴别甲烷与乙炔 | |
| B. | 用新制CaO检验乙醇中是否含有水分 | |
| C. | 用酸性KMnO4溶液直接检验乙醇与浓硫酸反应是否得到乙烯 | |
| D. | 取少量卤代烃加入NaOH水溶液共热,冷却,再加入AgNO3溶液检验卤代烃中卤原子的存在 |
17.下列物质的类别与所含官能团都正确的是( )
| A. |  酚类-OH | B. |  羧酸-COOH | C. |  醛类-CHO | D. | CH3COCH3 醚类 |
4. 向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀的物质的量(n)和加入溶液B的体积(V)关系如图.
向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀的物质的量(n)和加入溶液B的体积(V)关系如图.
(1)当加入B溶液110mL时,溶液中的沉淀为(化学式)BaSO4、Fe(OH)3
(2)从90mL至100 mL之间加入10mL B溶液时发生的离子反应方程式Al(OH)3+OH-=AlO2-+2H2O,Ba2++SO42-=BaSO4↓
(3)将A、B溶液中各溶质的物质的量浓度填入下表
 向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀的物质的量(n)和加入溶液B的体积(V)关系如图.
向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀的物质的量(n)和加入溶液B的体积(V)关系如图.(1)当加入B溶液110mL时,溶液中的沉淀为(化学式)BaSO4、Fe(OH)3
(2)从90mL至100 mL之间加入10mL B溶液时发生的离子反应方程式Al(OH)3+OH-=AlO2-+2H2O,Ba2++SO42-=BaSO4↓
(3)将A、B溶液中各溶质的物质的量浓度填入下表
| 溶质 | Na2SO4 | NaOH | BaCl2 | AlCl3 | FeCl3 |
| C(mol/L) |
1.设NA代表阿伏加德罗常数,下列叙述正确的是( )
| A. | 常温常压下,1molCO2与18gH2O所含有的原子总数均为3NA | |
| B. | 20℃时,1molSO2的体积一定大于22.4L | |
| C. | 1mol/LNaCl溶液表示1L水中含有NaCl58.5g | |
| D. | 标准状况下,11.2L NO与5.6 L O2形成的混合气体中含有的分子数为0.5NA |
18.锂电池是新一代高能电池,目前已研究出多种锂电池.某种锂电池的总反应式为:Li+MnO2═LiMnO2.下列说法中正确的是( )
| A. | Li是正极,MnO2是负极 | B. | 放电时正极的反应:Li-e-═Li+ | ||
| C. | 放电时正极的反应:MnO2+e-═MnO2- | D. | 电池放电时,产生高锰酸根离子 |
19.下列关于有机物的叙述正确的是( )
| A. | 乙醇不能发生取代反应 | |
| B. | C4H10有三种同分异构体 | |
| C. | 乙二醇和丙三醇为同系物 | |
| D. | 乙烯和甲烷可用溴的四氯化碳溶液鉴别 |
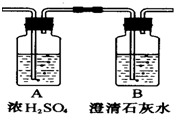 燃烧法是测定有机化合物化学式的一种重要方法.
燃烧法是测定有机化合物化学式的一种重要方法. 按官能团分类的类别是酚.
按官能团分类的类别是酚. 按官能团分类的类别是酯.
按官能团分类的类别是酯.