题目内容
17.根据下列实验操作和现象所得到的结论正确的是( )| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A |  | 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性:Cl2>Br2>I2 |
| B | 向某黄色溶液中加入淀粉KI溶液 | 溶液呈蓝色 | 溶液中含Br2 |
| C | 用大理石和盐酸反应制取CO2气体,立即通入一定浓度的Na2SiO3溶液中 | 出现白色沉淀 | H2CO3的酸性比H2SiO3的酸性强 |
| D | 向久置的Na2SO3溶液中加入足量BaCl2溶液,再加入足最稀盐酸 | 先出现白色沉淀,后部分沉淀溶解 | 部分Na2SO3被氧化 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.氯气可与NaBr、KI反应,干扰了检验结果;
B.该黄色溶液中可能含有铁离子,铁离子也能将碘离子氧化为碘单质;
C.盐酸为挥发性酸,盐酸能与硅酸钠溶液反应;
D.硫酸钡不溶于稀盐酸、亚硫酸钡溶于稀盐酸.
解答 解:A.氯气可与NaBr、KI反应,则该实验不能比较Br2、I2的氧化性,故A错误;
B.该黄色溶液中可能含有铁离子,铁离子也能将碘离子氧化为碘单质,所以不能确定该黄色溶液中含有溴,则结论不正确,故B错误;
C.盐酸为挥发性酸,盐酸能与硅酸钠溶液反应,则该实验不能比较碳酸、硅酸的酸性,故C错误;
D.硫酸钡不溶于稀盐酸、亚硫酸钡溶于稀盐酸,如果亚硫酸钠被氧化生成硫酸钠,则加入氯化钡产生白色沉淀,且向该白色沉淀中加入稀盐酸时部分沉淀不溶解,说明该白色沉淀中含有硫酸钡,则得出结论:部分Na2SO3被氧化,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及酸性比较、氧化还原反应、离子检验等,把握物质的性质及反应原理为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
7.中国古代涉及化学的叙述,下列解读错误的是( )
| A. | 《黄白第十六》中“曾青涂铁,铁赤如铜”'其“曾青”是铜盐 | |
| B. | 《汉书》中“高奴县有淆水可燃中的淆水指的是石油 | |
| C. | 《天工开物》中“凡石灰,经火焚炼为用”里的“石灰”指的是Ca(OH)2 | |
| D. | 《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的碱是碳酸钾 |
8.下列物质中,属于天然有机高分子化合物的是( )
| A. | 葡萄糖 | B. | 蔗糖 | C. | 淀粉 | D. | 塑料 |
5.下列化学用语表示正确的是( )
| A. | HClO的结构式:H-Cl-O | B. | NH4Cl的电子式为: | ||
| C. | CO2的比例模型: | D. | 甲烷的球棍模型: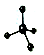 |
12.下列反应离子方程式正确的是( )
| A. | 钠和水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | NaHCO3溶液中加过量Ca(OH)2溶液:Ca2++2OH-+2HCO3-═CaCO3↓+CO32-+2H2O | |
| C. | 向氢氧化钡溶液中加入稀硫酸:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
11.下列关于有机化台物的说法正确的是( )
| A. | C3H2Cl6有4种同分异构体 | B. | 氯乙烯和聚乙稀均能发生加成反应 | ||
| C. |  的名称为异丁烷 的名称为异丁烷 | D. | C2H4和C4H8一定是同系物 |
8.下列说法正确的是( )
| A. | 只含有非金属元素的化合物一定是共价化合物 | |
| B. | NaOH、H2SO4溶于水均克服了离子键 | |
| C. | CO2、PCl3中所有原子最外层都满足8电子结构 | |
| D. | 金刚石和足球烯都属于原子晶体,熔化只克服共价键 |
9.将硫酸铝、硫酸钾和明矾溶液[KAl(SO4)2]等体积等浓度混合.该混合溶液中SO42-浓度为0.4mol/L.取100mL混合液加入0.4mol/L的KOH溶液,若要产生的沉淀量最大,加入该浓度的KOH的体积是( )
| A. | 100mL | B. | 150mL | C. | 200mL | D. | 250mL |

