题目内容
设NA表示阿伏加德罗常数,下列有关说法正确的是( )
| A、3.4g NH3中含N-H键数目为0.2 NA |
| B、标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0,.2 NA |
| C、7.8 g Na2O2含有的阴离子数目为0.2 NA |
| D、46g NO2和N2O4的混合气体中含有的原子个数为3NA |
考点:阿伏加德罗常数
专题:
分析:A、求出氨气的物质的量,然后根据1mol氨气中含3molN-H来分析;
B、氯气与氢氧化钠的反应为歧化反应;
C、求出Na2O2的物质的量,然后根据1molNa2O2含2mol钠离子和1mol过氧根来分析;
D、根据NO2和N2O4的最简式为CH2来分析.
B、氯气与氢氧化钠的反应为歧化反应;
C、求出Na2O2的物质的量,然后根据1molNa2O2含2mol钠离子和1mol过氧根来分析;
D、根据NO2和N2O4的最简式为CH2来分析.
解答:
解:A、3.4g氨气的物质的量n=
=
=0.2mol,而1mol氨气中含3molN-H键,故0.2mol氨气中含0.6molN-H键,故A错误;
B、标准状况下,2.24 L Cl2的物质的量为0.1mol,而氯气与氢氧化钠的反应为歧化反应,1mol氯气转移1mol电子,故0.1mol氯气转移0.1mol电子,故B错误;
C、7.8gNa2O2的物质的量为0.1mol,而1molNa2O2含2mol钠离子和1mol过氧根,故0.1mol过氧根中含0.1mol阴离子,故C错误;
D、NO2和N2O4的最简式为CH2,46g NO2和N2O4中含NO2的物质的量n=
=
=1mol,故含3mol原子,故D正确.
故选D.
| m |
| M |
| 3.4g |
| 17g/mol |
B、标准状况下,2.24 L Cl2的物质的量为0.1mol,而氯气与氢氧化钠的反应为歧化反应,1mol氯气转移1mol电子,故0.1mol氯气转移0.1mol电子,故B错误;
C、7.8gNa2O2的物质的量为0.1mol,而1molNa2O2含2mol钠离子和1mol过氧根,故0.1mol过氧根中含0.1mol阴离子,故C错误;
D、NO2和N2O4的最简式为CH2,46g NO2和N2O4中含NO2的物质的量n=
| m |
| M |
| 46g |
| 46g/mol |
故选D.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列有关碳和硅氧化物的说法中,正确的是( )
| A、二氧化硅的水溶液显酸性,所以,二氧化硅是酸性氧化物 |
| B、二氧化碳通入水玻璃可得到硅酸,说明碳酸的酸性比硅酸强 |
| C、高温时二氧化硅与纯碱反应放了二氧化碳,所以硅酸的酸性比碳酸强 |
| D、二氧化硅是酸性氧化物,因此,它不能溶于任何酸 |
下列化学用语正确的是( )
A、甲醛的电子式: |
B、异丙基的结构式: |
| C、甲醇的化学式:CH4O |
| D、乙醛的结构简式:CH3COH |
能正确表示下列反应的离子方程式是( )
| A、碳酸钙溶液和盐酸溶液混合:CO32-+2H+═CO2↑+H2O |
| B、硫酸溶液和氢氧化钠溶液混合:H++OH-═H2O |
| C、少量金属钠放入冷水中:Na+2H2O═Na++2OH-+H2↑ |
| D、铁与足量稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
下列反应最符合绿色化学原子经济性要求的是( )
①乙烷与氯气制备一氯乙烷
②乙烯聚合为聚乙烯高分子材料
③苯和硝酸反应制备硝基苯
④乙烯与氧气在银催化作用下生成环氧乙烷.
①乙烷与氯气制备一氯乙烷
②乙烯聚合为聚乙烯高分子材料
③苯和硝酸反应制备硝基苯
④乙烯与氧气在银催化作用下生成环氧乙烷.
| A、①④ | B、②④ | C、①③ | D、②③ |
把一套以液化石油气(主要成分为C3H8和C4H10)为燃料的炉灶,现改用天然气(主要成分为CH4)为燃料,需要调整进入炉灶的燃料气和空气的量.正确方法为( )
| A、同时调大燃料气和空气的量 |
| B、同时调小燃料气和空气的量 |
| C、只需调大燃料气的进气量 |
| D、只需调大空气的进气量 |
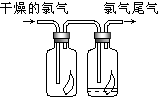 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是