题目内容
在密闭容器中进行如下反应:X2(g)+Y2(g)  2Z(g),已知X2、Y2、Z的起始浓度分别为0.2mol/L、0.4mol/L、0.3mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是 ( )
2Z(g),已知X2、Y2、Z的起始浓度分别为0.2mol/L、0.4mol/L、0.3mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是 ( )
A.X2为0.3mol/L B.Y为0.65mol/L C.Y2为0.2mol/L D.Z为0.7mol/L
A
【解析】
试题分析:【解析】
若反应向正反应进行到达平衡,X2、Y2的浓度最小,Z的浓度最大,假定完全反应,则:
X2(气)+Y2(气)?2Z(气),
开始(mol/L):0.2 0.4 0.3
变化(mol/L):0.2 0.2 0.4
平衡(mol/L):0 0.2 0.7
若反应逆正反应进行到达平衡,X2、Y2的浓度最大,Z的浓度最小,假定完全反应,则:
X2(气)+Y2(气)?2Z(气),
开始(mol/L):0.2 0.4 0.3
变化(mol/L):0.15 0.15 0.3
平衡(mol/L):0.3 5 0.55 0
由于为可逆反应,物质不能完全转化,所以平衡时浓度范围为0<c(X2)<0.35,0.2<c(Y2)<0.55,0<c(Z2)<0.7,选A.
考点:考查化学反应的可逆性。

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
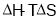 说法中正确的是( )
说法中正确的是( )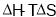 只用于判断温度、体积一定的反应能否自发进行
只用于判断温度、体积一定的反应能否自发进行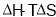 只用于判断温度、压强一定的反应能否自发进行
只用于判断温度、压强一定的反应能否自发进行 H+(溶液)+In-(溶液)
H+(溶液)+In-(溶液) nB(g)+nC(g)达平衡后,保持温度不变,将容器容积压缩到原来的一半,当达到新的平衡时,B和C的浓度均是原来的2.2倍,则 ( )
nB(g)+nC(g)达平衡后,保持温度不变,将容器容积压缩到原来的一半,当达到新的平衡时,B和C的浓度均是原来的2.2倍,则 ( )

