题目内容
17.下列离子方程式中,属于正确的水解反应的是( )| A. | HCO3-+H2O?H2CO3+OH- | B. | HS-+H2O?S2-+H3O+ | ||
| C. | CO32-+2H2O?H2CO3+2OH- | D. | F-+H2O═HF+OH- |
分析 水解离子反应中弱酸或弱碱离子结合水电离生成的氢离子或氢氧根离子生成弱电解质,以此分析.
解答 解:A、碳酸氢根离子的水解,结合水电离出的氢离,生成碳酸,所以水解的反应方程:HCO3-+H2O?H2CO3+OH-,故A正确;
B、硫氢根离子的电离方程式HS-+H2O?S2-+H3O+,而不是水解,故B错误;
C、水解是分步进行,第一步只能结合一个氢离子,水解反应的方程式:CO32-+H2O?HCO3-+OH-,故C错误;
D、盐的水解是可逆的,所以水解反应的方程式为:F-+H2O?HF+OH-,故D错误;
故选A.
点评 本题考查水解的离子反应,明确水解的反应原理是解答本题的关键,注意区分水解、电离的离子反应,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.下表中所示实验装置的图示或操作中,不能达到实验目的是( )
| A. | 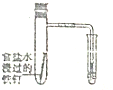 验证铁的析氢腐蚀 | B. | 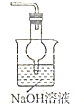 吸收SO2 | ||
| C. | 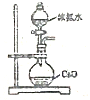 制取少量氨气 | D. | 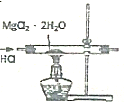 制取无水MgCl2 |
8.2015年10月5日,中国药学家屠呦呦因发现了青蒿素和双氢青蒿素获2015年诺贝尔生理学或医学奖.青蒿素分子式C15H22O5,含有7个手性碳原子.下列化合物中含有不止一个手性碳原子的是( )
| A. | CH3CHO | B. | CH2OH(CHOH)4CHO | C. | CH3CH2CH2OH | D. | CH3CH(OH)COOH |
5.下列气体不能用排空气法收集的是( )
| A. | NO | B. | NO2 | C. | SO2 | D. | NH3 |
12.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 常温常压下,32 g O3含有的氧原子数目为2 NA | |
| B. | 56 g的Fe与足量的稀盐酸完全反应转移电子数为3NA | |
| C. | 0.1 mol•L-1Na2SO4溶液含有的钠离子数目为0.2 NA | |
| D. | 标准状况下,22.4 L 四氯化碳(CCl4)含有的碳原子数目为NA |
2.在0.1mol•L-1 Na2S溶液中,下列关系式正确的是( )
| A. | c(Na+)>c(OH-)>c(HS-)>c(S2-) | B. | c(Na+)+c(H+)=c(HS-)+c(S2-)+c(OH-) | ||
| C. | 2c(Na+)=c(H2S)+c(HS-)+c(S2-) | D. | c(OH-)=c(H+)+c(HS-)+2c(H2S) |
9.下列反应的离子方程式正确的是( )
| A. | 碳酸钙溶于盐酸:CO32-+2H+═H2O+CO2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | FeCl3溶液中加入铁粉:Fe+Fe3+═2Fe2+ | |
| D. | 过氧化钠遇水:2Na2O2+2H2O═4Na++4OH-+O2↑ |
6.下表是某地区市场上销售的一种“加碘食盐”包装袋上的部分文字说明.请根据此表,结合化学和生物学科的知识,回答下列问题.
(1)要在食盐中加碘,是因为碘是人体内合成甲状腺激素的主要原料,缺碘会引起疾病.
(2)食盐中加碘,这碘指的是碘酸钾.碘酸钾的化学式为KIO3,其中碘元素的化合价为+5.
(3)根据含碘盐的食用方法,可推测碘酸钾在受热时容易分解.
| 配料表 | 精制海盐、碘酸钾 |
| 含碘量 | 20~40mg/kg |
| 卫生许可证号 | ××卫碘字(1999)第001号 |
| 分装日期 | 见封底 |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
(2)食盐中加碘,这碘指的是碘酸钾.碘酸钾的化学式为KIO3,其中碘元素的化合价为+5.
(3)根据含碘盐的食用方法,可推测碘酸钾在受热时容易分解.