题目内容
下列说法不正确的是( )
| A、1mol任何气体都含有NA个分子 |
| B、阿伏加德罗常数的“集体”就是1mol |
| C、摩尔是物质的量的单位,用于表示物质所含微粒多少 |
| D、阿伏加德罗常数的符号为NA,通常用6.02×1023表示 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、1mol粒子集体所含的微粒数即为阿伏伽德罗常数;
B、1mol粒子集体所含的微粒数即为阿伏伽德罗常数,故阿伏伽德罗常数个微粒,即为1mol;
C、物质的量表示的是一定数目粒子的集合体;
D、12g12C中含有的碳原子数即为阿伏伽德罗常数.
B、1mol粒子集体所含的微粒数即为阿伏伽德罗常数,故阿伏伽德罗常数个微粒,即为1mol;
C、物质的量表示的是一定数目粒子的集合体;
D、12g12C中含有的碳原子数即为阿伏伽德罗常数.
解答:
解:A、NA个微粒看成一个整体,就是1mol,故1mol任何气体都含有NA个分子,故A正确;
B、将阿伏加德罗常数个微粒看成一个整体,这个“集体”就是1mol,故B正确;
C、摩尔是物质的量的单位,用于表示含有一定数目粒子的集合体,故C错误;
D、将12g12C中含有的碳原子数称为阿伏加德罗常数,符号为NA,NA≈6.02×1023,故D正确.
故选C.
B、将阿伏加德罗常数个微粒看成一个整体,这个“集体”就是1mol,故B正确;
C、摩尔是物质的量的单位,用于表示含有一定数目粒子的集合体,故C错误;
D、将12g12C中含有的碳原子数称为阿伏加德罗常数,符号为NA,NA≈6.02×1023,故D正确.
故选C.
点评:本题主要考查了阿伏伽德罗常数的概念、阿伏伽德罗常数与与物质的量的关系,属于基本概念的考查,较简单.本题从阿伏伽德罗常数的概念、阿伏伽德罗常数与与物质的量的关系角度来分析.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
NA表示阿伏加德罗常数,下列判断正确的是( )
| A、25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| B、常温常压下,22.4LCO2中含有的CO2分子数小于NA个 |
| C、等物质的量的N2和CO的质量均为28g |
| D、常温下,1L 0.1mol/LNa2CO3溶液中,含有阴离子的总数小于0.1NA |
对于化学反应A+B=C+D的下列说法中,正确的是( )
| A、若生成物C和D分别为盐和水,则该反应一定是中和反应 |
| B、若A和C是单质,B和D是化合物,则该反应一定是置换反应 |
| C、若A是可溶性碱,B是可溶性盐,则C和D不可能是两种沉淀 |
| D、若A、B、C、D都是化合物,则该反应一定是复分解反应 |
下列物质的核磁共振氢谱图中,吸收峰最少的是( )
A、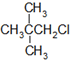 |
B、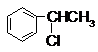 |
C、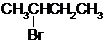 |
D、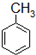 |
将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
①SO2+2Fe3++2H2O═SO42-+2Fe2++4H+
②Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
下列有关说法错误的是( )
①SO2+2Fe3++2H2O═SO42-+2Fe2++4H+
②Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
下列有关说法错误的是( )
| A、氧化性Cr2O72->Fe3+>SO2 |
| B、能将Na2SO3氧化成Na2SO4 |
| C、每有1 mol K2Cr2O7参加反应,转移电子的数目为3NA |
| D、若6.72 L SO2(标准状况)参加反应,则最终消耗0.1 mol K2Cr2O7 |
下列有关σ键和π键的说法错误的是( )
| A、含有π键的分子在反应时,π键是化学反应的积极参与者 |
| B、当原子形成分子时,首先形成σ键,可能形成π键 |
| C、有些原子在与其他原子形成分子时只能形成σ键,不能形成π键 |
| D、在分子中,化学键可能只有π键,而没有σ键 |
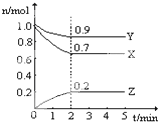 Ⅰ、A和B反应生成C,假定反应刚开始只有A、B,它们的起始浓度均为1mol/L.反应进行2min后A的浓度为0.8mol/L,B的浓度为0.6mol/L,C的浓度为0.6mol/L.则在这2min内反应的平均速率VA=
Ⅰ、A和B反应生成C,假定反应刚开始只有A、B,它们的起始浓度均为1mol/L.反应进行2min后A的浓度为0.8mol/L,B的浓度为0.6mol/L,C的浓度为0.6mol/L.则在这2min内反应的平均速率VA= X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y,X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y,X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.