题目内容
18.生命起源于海洋,科学家认为,由于海洋中Al3+的浓度极低,所以Al元素未成为人体内的必需元素,相反它对人体有害,下列有关铝的说法中不正确的是( )| A. | 家庭不宜用铝锅长期盛放菜,汤等食品 | |
| B. | 明矾[KAl(SO4)2•12H2O]含结晶水,是混合物 | |
| C. | Al既能与盐酸反应,又能与NaOH溶液反应 | |
| D. | 铝热反应是放热反应 |
分析 A.Al元素对人体有害;
B.明矾[KAl(SO4)2•12H2O]是含有结晶水的纯净物;
C.Al与酸、碱溶液可发生反应;
D.铝热反应是放热反应;
解答 解:A.Al元素对人体有害,所以不宜用铝合金容器长期存放菜、汤等食品,故A正确;
B.明矾[KAl(SO4)2•12H2O]含结晶水,但属于纯净物,故B错误;
C.铝为两性金属,所以既能与盐酸反应,又能与NaOH溶液反应,故C正确;
D.铝热反应在高温下反应的放热反应,故D正确;
故选B.
点评 本题考查物质的性质和用途,为高频考点,把握Al的化学性质及性质决定用途的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
8.下列关于合金的说法错误的是( )
| A. | 合金是由两种或两种以上的金属与非金属经一定方法所合成的具有金属特性的物质 | |
| B. | 镁铝合金的熔点比镁和铝都髙 | |
| C. | 在合金中加入适量的稀土金属能大大改善其性能 | |
| D. | 青铜、硬铝、钢都是合金 |
9.下列说法或表示方法不正确的是( )
| A. | 若形成化学键释放的能量大于断裂化学键所吸收的能量,则是放热反应 | |
| B. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ | |
| C. | 由4P(s,红磷)═P4(s,白磷)△H=+139.2 kJ/mol,可知红磷比白磷稳定 | |
| D. | 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ 热量,氢气燃烧的热化学方程式可表示为2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol |
6.下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1 mol•L-1某二元弱酸的酸式盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A) | |
| B. | 某酸式盐NaHY的水溶液显碱性,该酸式盐溶液中离子浓度关系为:c(Na+)>c(HY-)>c(OH-)>c(H+) | |
| C. | 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+c(OH-)=c(H+)+c(CH3COOH) | |
| D. | 25℃,pH=12的氨水和pH=2的盐酸等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
3.下列有关原电池的说法正确的是( )
| A. | 原电池是把电能转化为化学能的装置 | |
| B. | 原电池中电子流出的一极是负极,发生还原反应 | |
| C. | 构成原电池的两极必须是两种不同的金属 | |
| D. | Cu-Fe稀硫酸原电池工作时,铜是正极 |
10.将标准状况下的H2S气体通入100mL 5mol?L-1的CuSO4溶液中,再向混合溶液中滴加2mol?L-1NaOH溶液,当溶液的pH=7时,滴入的NaOH溶液体积为( )
| A. | 500mL | B. | 250mL | C. | 200mL | D. | 100mL |
7.柴静的调查报告《苍穹之下》引起人们对雾霾的更大关注.某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5微米的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样,测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断试样的pH=4.
(2)洗涤含SO2的烟气,下列物质可作洗涤剂的是bc
a.CaCl2 溶液 b.Na2CO3 溶液 c.Ca(OH)2 悬浊液 d.浓H2SO4
(3)安装汽车尾气催化转化器也可减轻PM2.5的危害,其反应是:
2NO(g)+2CO(g)$\frac{\underline{\;催化剂\;}}{\;}$2CO2(g)+N2(g);△H<0
①该反应平衡常数表达式K=$\frac{{c}^{2}(C{O}_{2})c({N}_{2})}{{c}^{2}(NO){c}^{2}(CO)}$;温度升高K值减小(填“增大”或“减小”)
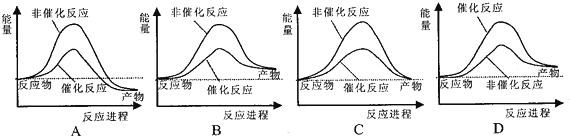
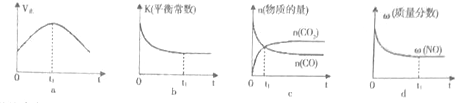
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是bd.
(4)汽车尾气中NOx和CO的生成及转化.
①已知汽缸中生成NO的反应为N2(g)+O2(g)?2NO(g)△H>0,汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是温度升高,平衡正向移动,NO的含量增大.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)═2C(s)+O2(g)△H>0,判断该设想能否实现:不能(填“能”或“不能”),简述其依据:;△H>0△S<0,则在任何温度下△G>0,不可能自发进行.
(1)将PM2.5样本用蒸馏水处理制成待测试样,测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离 子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)洗涤含SO2的烟气,下列物质可作洗涤剂的是bc
a.CaCl2 溶液 b.Na2CO3 溶液 c.Ca(OH)2 悬浊液 d.浓H2SO4
(3)安装汽车尾气催化转化器也可减轻PM2.5的危害,其反应是:
2NO(g)+2CO(g)$\frac{\underline{\;催化剂\;}}{\;}$2CO2(g)+N2(g);△H<0
①该反应平衡常数表达式K=$\frac{{c}^{2}(C{O}_{2})c({N}_{2})}{{c}^{2}(NO){c}^{2}(CO)}$;温度升高K值减小(填“增大”或“减小”)
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是bd.

(4)汽车尾气中NOx和CO的生成及转化.
①已知汽缸中生成NO的反应为N2(g)+O2(g)?2NO(g)△H>0,汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是温度升高,平衡正向移动,NO的含量增大.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)═2C(s)+O2(g)△H>0,判断该设想能否实现:不能(填“能”或“不能”),简述其依据:;△H>0△S<0,则在任何温度下△G>0,不可能自发进行.
8.下列是四种烷烃分子的结构模型图,其中沸点最高的是( )
| A. |  | B. | 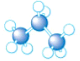 | C. | 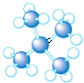 | D. |  |
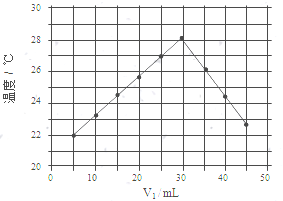 水不仅是包括人类在内所有生命生存的重要资源,也是化学反应中的重要物质:
水不仅是包括人类在内所有生命生存的重要资源,也是化学反应中的重要物质: