题目内容
20.用c(H+)均为0.01•L-1的盐酸和醋酸溶液,分别中和等体积.等物质的量浓度的氢氧化钠溶液,当氢氧化钠恰好被完全中和时,消耗盐酸和醋酸溶液的体积分别为Vl和V2,则Vl和V2的关系正确的是( )| A. | V1>V2 | B. | V1<V2 | C. | V1=V2 | D. | V1≤V2 |
分析 醋酸为弱酸,c(H+)均为0.01•L-1的盐酸和醋酸溶液,醋酸浓度大与盐酸,
分别中和等体积、等物质的量浓度的氢氧化钠溶液,当氢氧化钠恰好被完全中和时,消耗的两种酸的物质的量相等,
根据n=C×V比较二者的体积关系.
解答 解:醋酸为弱酸,c(H+)均为0.01•L-1的盐酸和醋酸溶液,醋酸浓度大与盐酸,
设盐酸的浓度为C1,醋酸的浓度为C2,则C1<C2,
分别中和等体积、等物质的量浓度的氢氧化钠溶液,当氢氧化钠恰好被完全中和时,消耗的两种酸的物质的量相等,
则有:n=C1V1=C2V2,
因C1<C2,
所以:V1>V2.
故选A.
点评 本题考查酸碱混合的定性判断,题目难度中等,本题注意醋酸为弱电解质这一特点.

练习册系列答案
相关题目
5.检验溶液中是否含有Fe3+可以用的试剂是( )
| A. | 稀HCl | B. | 蔗糖溶液 | C. | KSCN 溶液 | D. | NaCl 溶液 |
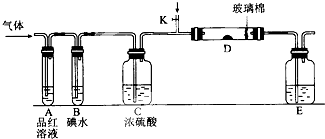 某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究S02和Cl2的性质.
某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究S02和Cl2的性质. 如图所示,甲、乙两池的电极材料都是铁棒与碳棒,丙池是电解精炼铜.
如图所示,甲、乙两池的电极材料都是铁棒与碳棒,丙池是电解精炼铜. 已知如图装置的甲、乙两室内装入液体的体积相同.请回答下列问题:
已知如图装置的甲、乙两室内装入液体的体积相同.请回答下列问题: