题目内容
11.C60可用作储氢材料.已知金刚石中的C-C的键长为154.45pm,C60中C一C键长为145〜140pm,有同学据此认为C60的熔点高于金刚石,你认为此说法是否正确,并阐述理由不正确,C60是分子晶体,熔化时不需破坏化学键.分析 不同晶体类型,其熔沸点比较要根据晶体类型判断高低,只有相同晶体类型时才考虑键长、键能大小对晶体熔沸点高低的影响,据此分析解答.
解答 解:金刚石是原子晶体而C60是分子晶体,尽管C60中C-C键长小于金刚石中键长,则C60中键的键能可能大于金刚石,但其熔化时并不破坏化学键,只破坏分子间作用力,而金刚石熔融时要破坏共价键,导致金刚石熔点高于C60,故答案:不正确,C60是分子晶体,熔化时不需破坏化学键.
点评 本题考查晶体熔沸点比较,为高频考点,明确晶体熔沸点与晶体类型、化学键关系是解本题关键,注意:不同晶体比较熔沸点时先比较晶体类型,如果晶体类型相同时再考虑键长、键能等,题目难度不大.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
1.根据键能与键长数据,推断下列分子的稳定顺序,正确的是( )
| 物质 | N2 | Cl2 | Br2 | I2 | O2 |
| 键能 (kJ•mol-1) | 945 | 243 | 193 | 151 | 498 |
| 键长(nm) | 0.110 | 0.199 | 0.228 | 0.266 | 0.121 |
| A. | N2>Cl2>Br2>O2>I2 | B. | O2>N2>I2>Br2>Cl2 | ||
| C. | I2>Br2>Cl2>O2>N2 | D. | N2>O2>Cl2>Br2>I2 |
2.下列说法正确的是( )
| A. | 能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 | |
| B. | 实验室制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体 | |
| C. | 单质硅是生产光纤制品的基本原料 | |
| D. | 水玻璃可用于生产黏合剂和防火剂 |
20.用c(H+)均为0.01•L-1的盐酸和醋酸溶液,分别中和等体积.等物质的量浓度的氢氧化钠溶液,当氢氧化钠恰好被完全中和时,消耗盐酸和醋酸溶液的体积分别为Vl和V2,则Vl和V2的关系正确的是( )
| A. | V1>V2 | B. | V1<V2 | C. | V1=V2 | D. | V1≤V2 |
1.实验室制备氯气,检验是否收集满的正确方法是( )
| A. | 用手扇动收集的气体,有气味则已收集满 | |
| B. | 将润湿的淀粉-KI试纸接近瓶口,试纸变蓝则已收集满 | |
| C. | 将润湿的红色石蕊试纸伸入瓶内,试纸腿色则已收集满 | |
| D. | 将铁丝伸到瓶口,铁丝燃烧说明已收集满 |
 最难
最难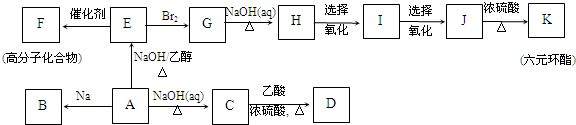
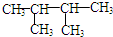 ,K为
,K为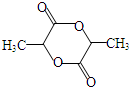 ;
;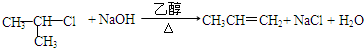 ;G→H
;G→H ;
;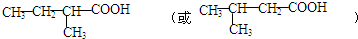 .
.