题目内容
(1)在反应NaClO+SO2+H2O=NaCl+H2SO4中,氧化剂是
在反应3NO2+H2O=2HNO3+NO中,还原产物是
(2)按要求写出下列反应的离子方程式
①氯气与氢氧化钙溶液反应:
②硫酸铝溶液与氨水反应:
③写出Ba(OH)2+NaHSO4=BaSO4↓+NaOH+H2O:
NaClO
NaClO
,氧化产物是H2SO4
H2SO4
;在反应3NO2+H2O=2HNO3+NO中,还原产物是
NO
NO
,氧化剂与还原剂的物质的量之比为1:2
1:2
.(2)按要求写出下列反应的离子方程式
①氯气与氢氧化钙溶液反应:
Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
;②硫酸铝溶液与氨水反应:
Al3++3NH3.H2O=Al(OH)3↓+3NH4+
Al3++3NH3.H2O=Al(OH)3↓+3NH4+
;③写出Ba(OH)2+NaHSO4=BaSO4↓+NaOH+H2O:
Ba2++OH-+H++SO42-=BaSO4↓+H2O
Ba2++OH-+H++SO42-=BaSO4↓+H2O
.分析:(1)氧化还原反应中得电子化合价降低的物质是氧化剂,失电子化合价升高的物质是还原剂,还原剂对应的产物是氧化产物,氧化剂对应的产物是还原产物.
(2)根据离子方程式的书写规则书写,注意弱电解质写化学式.
(2)根据离子方程式的书写规则书写,注意弱电解质写化学式.
解答:解:(1)在反应NaClO+SO2+H2O=NaCl+H2SO4中,NaClO中氯元素得电子化合价降低,所以次氯酸钠是氧化剂,二氧化硫中硫元素失电子化合价升高,二氧化硫是还原剂,氧化产物是硫酸,还原产物是氯化钠;在反应3NO2+H2O=2HNO3+NO中,二氧化氮中氮元素的化合价既有升高的也有降低的,所以二氧化氮既是氧化剂又是还原剂,还原产物是一氧化氮,氧化剂与还原剂的物质的量之比为1:2.
故答案为:NaClO;H2SO4;NO;1:2.
(2)①氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O.
故答案为:Cl2+2OH-=Cl-+ClO-+H2O.
②硫酸铝和氨水反应生成氢氧化铝和铵根离子,离子方程式为:Al3++3NH3.H2O=Al(OH)3↓+3NH4+.
故答案为:Al3++3NH3.H2O=Al(OH)3↓+3NH4+.
③硫酸氢钠和氢氧化钡反应的离子方程式为:Ba2++OH-+H++SO42-=BaSO4↓+H2O.
故答案为:Ba2++OH-+H++SO42-=BaSO4↓+H2O.
故答案为:NaClO;H2SO4;NO;1:2.
(2)①氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O.
故答案为:Cl2+2OH-=Cl-+ClO-+H2O.
②硫酸铝和氨水反应生成氢氧化铝和铵根离子,离子方程式为:Al3++3NH3.H2O=Al(OH)3↓+3NH4+.
故答案为:Al3++3NH3.H2O=Al(OH)3↓+3NH4+.
③硫酸氢钠和氢氧化钡反应的离子方程式为:Ba2++OH-+H++SO42-=BaSO4↓+H2O.
故答案为:Ba2++OH-+H++SO42-=BaSO4↓+H2O.
点评:本题考查了氧化剂和还原剂与氧化产物和还原产物的判断、离子方程式的书写,难度不大,注意硫酸氢钠在水溶液中电离生成钠离子、氢离子和硫酸根离子,为易错点.

练习册系列答案
相关题目
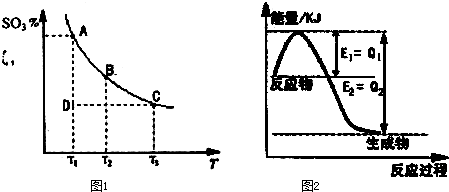
 2SO3(g)的混合体系中,SO3的百分含量和温度的关系如下图(曲线上任何一点都表示平衡状态):
2SO3(g)的混合体系中,SO3的百分含量和温度的关系如下图(曲线上任何一点都表示平衡状态):
