题目内容
写出下列反应的化学方程式或离子方程式.
(1)1g乙醇C2H5OH完全燃烧放出热量12kJ,写出表示乙醇燃烧热的热化学方程式:
(2)用惰性电极电解CuSO4溶液的化学方程式:
(3)钢铁发生吸氧腐蚀的正极反应:
(4)AmBn是强碱弱酸盐,写出Bm-水解的离子方程式:
(5)电解饱和食盐水阴极室所发生的电极反应: .
(1)1g乙醇C2H5OH完全燃烧放出热量12kJ,写出表示乙醇燃烧热的热化学方程式:
(2)用惰性电极电解CuSO4溶液的化学方程式:
(3)钢铁发生吸氧腐蚀的正极反应:
(4)AmBn是强碱弱酸盐,写出Bm-水解的离子方程式:
(5)电解饱和食盐水阴极室所发生的电极反应:
考点:离子方程式的书写
专题:离子反应专题
分析:(1)依据1g乙醇完全燃烧生成CO2和液态水时放热12kJ,结合燃烧热的定义计算求出1mol乙醇完全燃烧放出的热量,然后写出热化学方程式;
(2)用惰性电极电解硫酸铜溶液时,阳极上氢氧根离子放电、阴极上铜离子放电,电解生成金属铜,硫酸和氧气;
(3)钢铁发生吸氧腐蚀的正极反应得到电子;
(4)Bm-水解为多元弱酸的酸式根离子,分步水解,以第一步水解为主,水解生成氢氧根离子和HB(m-1)-;
(5)阴极发生还原反应,水在阴极放电生成氢气与氢氧根离子.
(2)用惰性电极电解硫酸铜溶液时,阳极上氢氧根离子放电、阴极上铜离子放电,电解生成金属铜,硫酸和氧气;
(3)钢铁发生吸氧腐蚀的正极反应得到电子;
(4)Bm-水解为多元弱酸的酸式根离子,分步水解,以第一步水解为主,水解生成氢氧根离子和HB(m-1)-;
(5)阴极发生还原反应,水在阴极放电生成氢气与氢氧根离子.
解答:
解:(1)1g乙醇完全燃烧生成CO2和液态水时放热12kJ,则1mol乙醇,质量为46g,完全燃烧生成稳定的氧化物放出的热量为:46×12kJ=552KJ,
其燃烧热的热化学方程式为:C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H=-552 kJ?mol-1;
(2)用惰性电极电解硫酸铜溶液时,阳极上氢氧根离子放电生成氧气、阴极上铜离子放电生成Cu,化学方程式为2CuSO4+2H2O
2Cu+O2↑+2H2SO4
故答案为:2CuSO4+2H2O
2Cu+O2↑+2H2SO4;
(3)钢铁发生吸氧腐蚀的正极反应式为O2+4e-+2H2O═4OH-,
故答案为:O2+4e-+2H2O═4OH-;
(4)Bm-水解为多元弱酸的酸式根离子,分步水解,以第一步水解为主:Bm-+H2O OH-+HB(m-1)-;
OH-+HB(m-1)-;
故答案为:Bm-+H2O OH-+HB(m-1)-;
OH-+HB(m-1)-;
(5)电解饱和食盐水阴极室所发生的电极反应:2H2O+2e-=2OH-+H2↑,故答案为:2H2O+2e-=2OH-+H2↑.
其燃烧热的热化学方程式为:C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H=-552 kJ?mol-1;
(2)用惰性电极电解硫酸铜溶液时,阳极上氢氧根离子放电生成氧气、阴极上铜离子放电生成Cu,化学方程式为2CuSO4+2H2O
| ||
故答案为:2CuSO4+2H2O
| ||
(3)钢铁发生吸氧腐蚀的正极反应式为O2+4e-+2H2O═4OH-,
故答案为:O2+4e-+2H2O═4OH-;
(4)Bm-水解为多元弱酸的酸式根离子,分步水解,以第一步水解为主:Bm-+H2O
 OH-+HB(m-1)-;
OH-+HB(m-1)-;故答案为:Bm-+H2O
 OH-+HB(m-1)-;
OH-+HB(m-1)-;(5)电解饱和食盐水阴极室所发生的电极反应:2H2O+2e-=2OH-+H2↑,故答案为:2H2O+2e-=2OH-+H2↑.
点评:本题考查了离子方程式的书写,明确反应的实质、原电池、电解池工作原理是解题关键,题目难度不大.

练习册系列答案
相关题目
在相同温度下,pH相同的盐酸和碳酸的说法正确的是( )
| A、氢氧化钠中和等体积该条件下的盐酸和碳酸时,盐酸消耗的氢氧化钠多 |
| B、相同体积的盐酸和碳酸与足量的亚硫酸氢钠反应时,碳酸产生的SO2多 |
| C、两溶液的导电能力几乎相同 |
| D、溶液中离子总数一定不相等 |
“84”消毒液在日常生活中被广泛应用.该消毒液无色,pH大于7,对某些有色物质有漂白作用.你认为它可能的有效成分是( )
| A、SO2 |
| B、Na2CO3 |
| C、KMnO4 |
| D、NaClO |
HCN无色有杏仁气味的有毒气体,早期广泛用于船舱、仓库的烟熏灭鼠.已知:HCN( aq)与NaOH(aq)反应的焓变△H=-12.1kJ?mol-1; HCl(aq)与NaOH(aq)反应的焓变△H=-55.6kJ?mol-1.则HCN在水溶液中电离的焓变△H等于( )
| A、-67.7 kJ?mol-1 |
| B、-43.5 kJ?mol-1 |
| C、+43.5 kJ?mol-1 |
| D、+67.7 kJ?mol-1 |
下列叙述中正确的是( )
| A、在稀溶液中,1mol酸和1mol碱完全反应所放出的热量,叫作中和热 |
| B、在101kpa时,1mol物质燃烧时所放出的热量叫作该物质的燃烧热 |
| C、热化学方程式中,各物质前的化学计量数不表示分子个数 |
| D、已知S(s)+O2(g)=SO2(g)△H1;S(g)+O2(g)=SO2(g)△H2,则△H1<△H2 |
下列关于热化学反应的描述中正确的是( )
| A、HCl和NaOH反应的中和热△H=-57.3kJ?mol-1,则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ?mol-1 |
| B、CO(g)的燃烧热是283.0 kJ?mol-1,则2CO2(g)=2CO(g)+O2(g)反应的△H=+2×283.0 kJ?mol-1 |
| C、需要加热才能发生的反应一定是吸热反应 |
| D、乙烷的燃烧热就是1mol乙烷燃烧生成气态水和二氧化碳所放出的热量 |
下列推论正确的是( )
| A、S(g)+O2(g) SO2(g)△H1; S(s)+O2(g)=SO2(g)△H2,则:△H1>△H2 |
| B、C(石墨,S)=C(金刚石,S)△H=+l.9 kJ/mol,则由石墨制取金刚石的反应是吸热反应,金刚石比石墨稳定 |
| C、NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(1)△H=-57.4 kJ/mol,则:含20 gNaOH的稀溶液与稀盐酸完全反应,放出的热量为28.7 kJ |
| D、2C(s)+O2(g)=2CO(g)△H=-221kJ/mol,则碳的燃烧热等于110.5kJ/mol |
下列化学用语正确的是( )
A、乙酸根离子的结构式: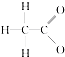 |
| B、乙酸的结构简式C2H4O2 |
| C、3-甲基-1-丁烯的结构简式:(CH3)2CHCH═CH2 |
D、醛基的电子式: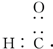 |