题目内容
16. 央视3.15晚会曝光在液化石油气中掺混二甲醚的事件.二甲醚(常压下沸点-24.9℃)是一种可溶于水的化工原料,常被用作一些燃料的替代品,其结构式如图.下列有关二甲醚的叙述中正确的是( )
央视3.15晚会曝光在液化石油气中掺混二甲醚的事件.二甲醚(常压下沸点-24.9℃)是一种可溶于水的化工原料,常被用作一些燃料的替代品,其结构式如图.下列有关二甲醚的叙述中正确的是( )| A. | 二甲醚是一种有机物,属于非电解质 | |
| B. | 4.6g该物质中含有共价键的数目为7×6.02×1022 | |
| C. | 二甲醚与甲醇(CH3OH)互为同系物 | |
| D. | 0.5mol二甲醚完全燃烧生成22.4LCO2 |
分析 A.在水溶液里和熔融状态下不导电的化合物是非电解质;
B.一个二甲醚分子中含有共价键数目是8个,4.6g二甲醚的物质的量为$\frac{4.6g}{46g/mol}$=0.1mol;
C.分子式相同结构不同的有机物互为同分异构体;结构相似,在分子组成上相差一个或n个-CH2原子团的有机物互称同系物;
D.没有指出标况下,不能使用标况下的气体摩尔体积计算生成二氧化碳的体积.
解答 解:A.在水溶液里和熔融状态下不导电的化合物是非电解质,二甲醚是有机物,不溶于水,在水中以分子存在,所以属于非电解质,故A正确;
B.一个二甲醚分子中含有共价键数目是8个,4.6g二甲醚的物质的量为$\frac{4.6g}{46g/mol}$=0.1mol,则4.6g该物质中含有共价键的数目为8×6.02×1022,故B错误;
C.分子式相同结构不同的有机物互为同分异构体,所以二甲醚和乙醇是同分异构体;结构相似,在分子组成上相差一个或n个-CH2原子团的有机物互称同系物,但和甲醇不属于同系物,故C错误;
D.不是标况下,不能使用标况下的气体摩尔体积计算,故D错误;
故选A.
点评 本题考查有机物结构和性质,涉及同系物、同分异构体、非电解质、物质的量的计算等知识,熟悉概念内涵是解本题关键,同分异构体的书写或同分异构体种类的判断是高考高频点,易错选项是D.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
6.下列表达正确的是( )
| A. | N2的电子式为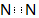 | B. | H2S的电子式可表示为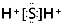 | ||
| C. | 用电子式表示Na2O的形成过程为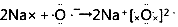 | D. | MgCl2的电子式为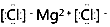 |
7.下列分子中只存在σ键的是( )
| A. | CS2 | B. | SiH4 | C. | C2H2 | D. | O2 |
4.已知反应:2NO2(红棕色)?N2O4(无色),分别进行如下两个实验:
实验ⅰ:将NO2球分别浸泡在热水和冰水中,现象如图1.
实验ⅱ:将一定量的NO2充入注射器中后封口,测定改变注射器体积的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),如图2.下列说法不正确的是( )

实验ⅰ:将NO2球分别浸泡在热水和冰水中,现象如图1.
实验ⅱ:将一定量的NO2充入注射器中后封口,测定改变注射器体积的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),如图2.下列说法不正确的是( )

| A. | 图1现象说明该反应为放热反应 | |
| B. | 图2中b点的操作是压缩注射器体积 | |
| C. | c点:v (正)<v (逆) | |
| D. | 若不忽略体系温度变化,且没有能量损失,则T(d)>T(c) |
11.以下反应最符合绿色化学原子经济性要求的是( )
①乙烷与氯气制备一氯乙烷,②乙烯聚合为聚乙烯高分子材料,③苯和硝酸反应制备硝基苯.④乙烯与氧气在银催化作用下生成环氧乙烷(C2H4O)
①乙烷与氯气制备一氯乙烷,②乙烯聚合为聚乙烯高分子材料,③苯和硝酸反应制备硝基苯.④乙烯与氧气在银催化作用下生成环氧乙烷(C2H4O)
| A. | 只有②④ | B. | 只有①③ | C. | 只有②③ | D. | 只有①④ |
1.下列各组物质所属类型全部正确的是( )
| A. | 碱性氧化物:Na2O Na2O2 A12O3 | B. | 酸性氧化物:CO SiO2 SO2 | ||
| C. | 盐:NH4NO3 KA1(SO4)2 KHSO4 | D. | 碱:烧碱 纯碱 碱石灰 |
6.下列过程属于物理变化的是( )
| A. | 碳在氧气中燃烧 | B. | 石油的分馏 | C. | 煤的干馏 | D. | 金属钠溶于水 |
3.化学与能源开发、环境保护、资源利用等密切相关.下列说法正确的是( )
| A. | 天然气、石油、流水、风力、氢气为一次能源 | |
| B. | 无论是风力发电还是火力发电,都是将化学能转化为电能 | |
| C. | PM2.5含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素 | |
| D. | 垃圾是放错地方的资源,应分类回收利用 |
4.常温下,Ka (HCOOH)=1.77×10-4,Ka (CH3COOH)=1.75×10-5,下列说法正确的是( )
| A. | 用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液至终点,消耗NaOH溶液的体积相等 | |
| B. | 浓度均为0.1 mol•L-1的 HCOONa和NaCl溶液中阴离子的物质的量浓度之和:前者大于后者 | |
| C. | 0.2 mol•L-1 CH3COONa 与 0.1 mol•L-1盐酸等体积混合后的溶液 (pH<7)中,某些粒子浓度大小关系:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| D. | 0.4 mol•L-1 HCOOH 与 0.2 mol•L-1 NaOH 等体积混合后的溶液中,某些粒子浓度大小关系:c(HCOO-)+c(OH-)=c(HCOOH)+c(H+) |