题目内容
16.某3.65g气在标准状况下的体积是2.24L,则其摩尔质量是36.5g/mol.分析 根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$计算.
解答 解:根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$,可知M=$\frac{m•{V}_{m}}{V}$=$\frac{3.65g×22.4L/mol}{2.24L}$=36.5g/mol;故答案为:36.5g/mol.
点评 本题考查了摩尔质量的概念和计算方法,注意摩尔质量是由单位的,单位为g/mol.

练习册系列答案
相关题目
6.“绿色化学”要求从经济、环保和技术上设计可行的化学反应.据此,由单质镁制硝酸镁的下列4个方案中,你认为可行而且符合“绿色化学”要求的方案是( )
| A. | Mg$\stackrel{浓HNO_{3}}{→}$Mg(NO3)2 | |
| B. | Mg$\stackrel{Cl_{2}}{→}$MgCl2$\stackrel{NaOH}{→}$Mg(OH)2$\stackrel{稀HNO_{3}}{→}$Mg(NO3)2 | |
| C. | Mg$\stackrel{O_{2}}{→}$MgO$\stackrel{稀HNO_{3}}{→}$Mg(NO3)2 | |
| D. | Mg$\stackrel{浓H_{2}SO_{4}}{→}$MgSO4$\stackrel{Ba(NO_{3})_{2}溶液}{→}$Mg(NO3)2 |
4.某有机物的结构简式为 ,关于它的叙述不正确的是( )
,关于它的叙述不正确的是( )
 ,关于它的叙述不正确的是( )
,关于它的叙述不正确的是( )| A. | 该有机物能使溴的CCl4溶液褪色 | |
| B. | 该有机物在一定条件下可发生加聚反应,生成高分子化合物(C7H10O5)n | |
| C. | 该有机物在一定条件下可发生氧化反应 | |
| D. | 该有机物发生消去反应可得芳香烃 |
3.点燃某气体后,在火焰上方罩一个冷烧杯,内壁有水珠出现,罩一个沾有澄清石灰水的烧杯,石灰水变浑浊,则该气体不可能是( )
| A. | 天然气 | B. | 液化石油气 | C. | 水煤气 | D. | 氢气 |
4.将过量铁粉放入100mL 2mol/L的HNO3溶液中,假设还原产物只有NO且HNO3完全反应,则参加反应的Fe的质量为( )
| A. | 2.8 g | B. | 5.6 g | C. | 4.2 g | D. | 11.2 g |
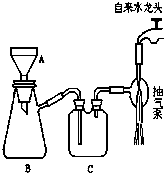 如图所示为减压过滤装置,回答有关问题.
如图所示为减压过滤装置,回答有关问题.