题目内容
11.题目科学家经过数学计算后,认为可能存在H3分子,1996年科学家在宇宙中发现了H3分子.假定,这三个氢原子的成键情况完全相同,则H3的几何形状应是正三角形;如果只有两个氢原子的成键情况相同,则H3的几何形状应是线型.分析 一般来说,活泼金属与非金属形成离子键,同种非金属之间形成非极性共价键,不同非金属元素之间形成极性共价键,三个氢原子的成键情况完全相同,形成非极性键,H3的几何形状应是正三角形.如果只有两个氢原子的成键,则为线型.
解答 解:1个H3分子由3个氢原子构成,三个氢原子的成键情况完全相同,形成非极性键,则H3的几何形状应是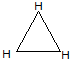 ,正三角形,如果只有两个氢原子的成键情况相同,则H3的几何形状应是H-H-H,为线型,
,正三角形,如果只有两个氢原子的成键情况相同,则H3的几何形状应是H-H-H,为线型,
故答案为:正三角形;线型.
点评 本题考查了分子的立体构型的判断,侧重分子结构与性质的考查,注意极性键的理解应用,题目难度中等.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
1.利用如图装置,完成很多电化学实验.下列有关此装置的叙述中,正确的是( )


| A. | 若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阴极的阳极保护法 | |
| B. | 若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动 | |
| C. | 若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阴离子向铁电极移动 | |
| D. | 若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小 |
2.如图为海水综合利用的工业流程图,判断下列说法正确的是( )

| A. | 过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 | |
| B. | 在过程③中将MgCl2•6H2O灼烧即可制得无水MgCl2 | |
| C. | 在过程④、⑥反应中每氧化0.2 mol Br-需消耗0.1mol Cl2 | |
| D. | 除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
3.将10mL 0.3mol•L-1的氨水与30mL 0.1mol•L-1的醋酸混合,溶液恰好显中性,下列结论正确的是( )
| A. | 原溶液中氨水中的c(OH-)与醋酸中的c(H+)相等 | |
| B. | CH3COONH4不发生分解 | |
| C. | 混合溶液中,c(NH3•H2O)=c(CH3COOH) | |
| D. | Kb(NH3•H2O)=3Ka(CH3COOH) |
11.将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入0.5L密闭容器内,550℃时,在催化剂作用下发生反应:2SO2(g)+O2(g)$?_{△}^{催化剂}$ 2SO3(g)(正反应放热).测得n(O2)随时间的变化如下表
4s后反应达到平衡,将容器中的混合气体通过过量NaOH溶液,气体体积减少了22.4L(此体积为标准状况下的体积);再将剩余气体通过焦性没食子酸的碱性溶液吸收O2(提示:焦性没食子酸的碱性溶液可以吸收O2),气体的体积又减少了5.6L(此体积为标准状况下的体积).请回答下列问题:
(1)用O2表示从0~2s内该反应的平均反应速率为0.4mol•L-1•s-1.
(2)O2的平衡浓度c(O2)=0.5mol•L-1.
(3)求该反应达到平衡时SO2的转化率是90%(用百分数表示).
(4)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀10.5克(计算结果保留一位小数).
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(O2)/mol | 0.7 | 0.4 | 0.3 | x | x | x |
(1)用O2表示从0~2s内该反应的平均反应速率为0.4mol•L-1•s-1.
(2)O2的平衡浓度c(O2)=0.5mol•L-1.
(3)求该反应达到平衡时SO2的转化率是90%(用百分数表示).
(4)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀10.5克(计算结果保留一位小数).
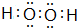 该物质能使酸性KMnO4溶液褪色,在这个反应中体现了该物质的还原性(填“氧化性”或“还原性”)
该物质能使酸性KMnO4溶液褪色,在这个反应中体现了该物质的还原性(填“氧化性”或“还原性”)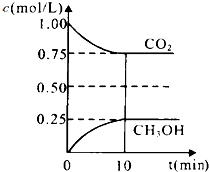 碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式.在一定温度下的2L固定容积的密闭容器中,通入2molCO2和3mol H2,发生的反应为:CO2(g)+3H2(g)CH3OH(g)+H2O(g),△H=-a kJ•mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式.在一定温度下的2L固定容积的密闭容器中,通入2molCO2和3mol H2,发生的反应为:CO2(g)+3H2(g)CH3OH(g)+H2O(g),△H=-a kJ•mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.