题目内容
1.下列金属中,既能与氯气反应又能和盐酸反应,且生成相同氯化物的是( )| A. | Fe | B. | Cu | C. | Mg | D. | Ag |
分析 能与盐酸反应的金属应为活泼金属,且与氯气反应生成相同的氯化物,说明金属不存在多种化合价,以此解答该题.
解答 解:A.Fe与盐酸反应生成FeCl2,与氯气反应生成FeCl3,生成的氯化物不同,故A错误;
B.Cu与盐酸不反应,与氯气反应生成氯化铜,故B错误;
C.Mg与盐酸或氯气反应都生成MgCl2,生成的氯化物相同,故C正确;
D.Ag与盐酸不反应,与氯气反应都生成AgCl,故D错误.
故选C.
点评 本题考查氯气的性质,侧重于基础知识的考查,注意常见金属的性质以及盐酸和氯气的氧化性的不同,难度不大,学习中注意相关基础知识的积累.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
11.对于相同物质的量的S02和S03,下列说法中正确的是( )
| A. | 氧元素的质量比为1:1 | B. | 质量之比为1:1 | ||
| C. | 原子总数之比为1:1 | D. | 硫元素的质量比为1:1 |
9.下列实验现象的描述错误的是( )
| A. | 氢气在氯气中燃烧生成黄绿色烟雾 | |
| B. | 红热的铁丝在氧气中燃烧,火星四射,生成黑色固体颗粒 | |
| C. | 点燃的硫在氧气中剧烈燃烧,发出蓝紫色火焰 | |
| D. | 钠在空气中燃烧,发出黄色的火焰,生成淡黄色固体 |
6.下列物质能导电且属于电解质的是 ( )
| A. | 铁 | B. | 盐酸 | C. | 氯化钠晶体 | D. | 熔融氢氧化钠 |
13.已知,还原性HSO3->Cl-,氧化性ClO3->Cl2.
实验Ⅰ:在一定量NaHSO3的溶液中逐滴加入KClO3溶液至过量;
实验Ⅱ:在一定量的KClO3溶液中逐滴加NaHSO3溶液至过量,下列说法正确的是( )
实验Ⅰ:在一定量NaHSO3的溶液中逐滴加入KClO3溶液至过量;
实验Ⅱ:在一定量的KClO3溶液中逐滴加NaHSO3溶液至过量,下列说法正确的是( )
| A. | 实验Ⅰ中溶液的酸性不断增强 | |
| B. | 两实验中生成等量Cl2时,转移电子数的物质的量相同 | |
| C. | 在实验Ⅰ的过程中,若NaHSO3初始量为3mol,当溶液中Cl-与Cl2的物质的量之比为5:2时,氧化产物为3.2mol | |
| D. | 试验Ⅱ反应结束后,加入碘化钾溶液,溶液呈蓝色 |
10.在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.01mol的混合溶液中加入0.01mol铁粉,经搅拌后发生的变化应是( )
| A. | 铁溶解,析出0.01molAg和0.005 molCu | |
| B. | 铁溶解,析出0.01molAg并放出H2 | |
| C. | 铁溶解,析出0.01molAg,溶液中不再有Fe3+ | |
| D. | 铁溶解,析出0.01molAg,溶液中不再有Cu2+ |
11.下列溶液中各微粒的浓度关系正确的是( )
| A. | NH4Cl溶液中:c(Cl-)=c(NH4+)>c(OH-)=c(H+) | |
| B. | Na2SO4溶液中:c(Na+)+c(H+)=c(SO42-)+c(OH-) | |
| C. | NaHCO3溶液中:c(Na+)>c(HCO3-)>c(H+)>c(OH-) | |
| D. | 等体积、等物质的量浓度的CH3COONa和弱酸CH3COOH混合后的溶液中:c(CH3COO-)-c(CH3COOH)=2c(H+)-2c(OH-) |

 .
.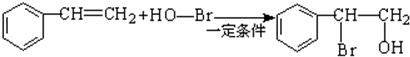 .
.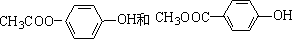 .
. )的合成线路:
)的合成线路: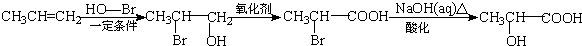 .
.