题目内容
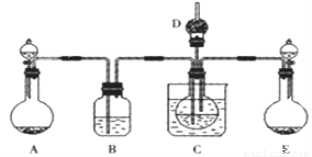
部分氧化的Fe?Cu合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理:

下列说法正确的是
A.滤液A中的阳离子为Fe2+、Fe3+、H+ B.样品中CuO的质量为4.0 g
C.V=448 D.原样品中Fe元素的质量分数为41%
C
【解析】
试题分析: 合金样品中含有金属铁、氧化铁、氧化铜、金属铜,金属铁、氧化铁、氧化铜都可以和硫酸反应,但金属铜不能反应,但是Cu却可以和和Fe3+反应,样品和足量的稀硫酸反应,因硫酸足量,放出的VmL气体为氢气,生成的滤渣3.2g是铜,滤液中的铁元素,在加入氢氧化钠后全部变成氢氧化铁,灼烧后变为3.2g为三氧化二铁,n(Fe2O3)=3.2g÷160g/mol=0.02mol。A.生成的3.2g滤渣是铜,金属铜可以和Fe3+发生反应2Fe3++Cu═2Fe2++Cu2+,所以滤液中一定不含有Fe3+,故选项A错误; B.固体3.2g为三氧化二铁,其物质的量为 n(Fe2O3)=3.2g÷160g/mol=0.02mol。在原固体中Fe的物质的量是n(Fe)= 0.04mol,其质量是0.04mol×56g/mol=2.24g,而原来固体5.76g,所以CuO质量不超过5.76-2.24=3.52g,故选项B错误;原样品中Fe元素的质量分数为(2.24g ÷5.76 g )×100%=39%,因此选项D错误;由于最后溶液中溶质为过量H2SO4和FeSO4,而铁元素物质的量为0.04mol,说明参加反应硫酸物质的量为0.04mol,则n(H+)=0.08mol,其中部分氢离子生成氢气,另外的H+和合金中的氧结合成水了,在合金中氧元素物质的量是(5.76-3.2-2.24) g÷ 16g/mol=0.02mol,它结合氢离子产生水消耗H+的物质的量为0.04mol,故产生氢气的H+:n(H+)=(0.08-0.04)mol=0.04mol因此生成0.02mol氢气,在标况下其体积为448ml,故现象D正确。
考点:考查混合物中物质成分和含量的确定的知识。

 阅读快车系列答案
阅读快车系列答案 ,则X、W可能是( )
,则X、W可能是( ) cC(g)+dD(g) ΔH的有关图像如下:
cC(g)+dD(g) ΔH的有关图像如下:
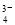 +2I-+2H+
+2I-+2H+ AsO
AsO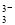 +I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。下列叙述中正确的是
+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。下列叙述中正确的是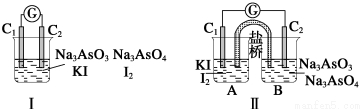
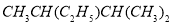 的名称是 。
的名称是 。