题目内容
下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO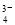 +2I-+2H+
+2I-+2H+ AsO
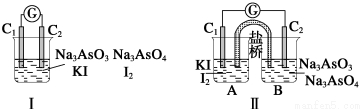
AsO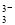 +I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。下列叙述中正确的是
+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。下列叙述中正确的是
A.甲组操作时,电流计(G)指针发生偏转
B.甲组操作时,溶液颜色变浅
C.乙组操作时,C2做正极
D.乙组操作时,C1上发生的电极反应为
I2+2e-===2I-
D
【解析】
试题分析:A.甲组操作时,两个电极均为碳棒,不能发生原电池反应,电流计(G)指针不会发生偏转,错误; B.发生反应生成碘单质,则溶液颜色加深,故选项B错误;C.乙组操作时,As元素失去电子,C2做负极,故C错误; D.乙组操作时,C1上得到电子,为正极,发生的电极反应为I2+2e-═2I-,正确。
考点:考查电化学反应原理的知识。

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
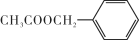 )是其中的一种,它可以从茉莉花中提取。一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取。一种合成路线如下: 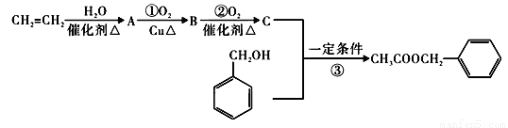
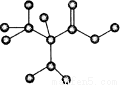
 Fe(s)+CO2(g) ΔH=a kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是
Fe(s)+CO2(g) ΔH=a kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是
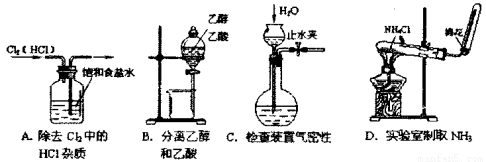
 和
和 
