题目内容
5.下列反应属于盐类水解反应且表达正确的是( )| A. | CO32-+2H2O?H2CO3+2OH- | |
| B. | CH3COOH+OH-═CH3COO-+H2O | |
| C. | 碳酸氢钠溶液:HCO3-+H2O?CO32-+H3O+ | |
| D. | Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3H+ |
分析 含有弱酸、弱碱对应的离子的盐易发生水解反应,强酸弱碱盐水解呈酸性,强碱弱酸盐水解呈碱性,多元弱酸的酸性离子发生多步水解,以第一步水解为主,注意电离和水解的区别,以此解答该题.
解答 解:A.以第一步水解为主,应为CO32-+H2O?HCO3-+OH-,故A错误;
B.为酸碱中和反应,故B错误;
C.水解呈碱性,应为HCO3-+H2O?H2CO3+OH-,故C错误;
D.铁离子水解呈酸性,同时生成氢氧化铁,故D正确.
故选D.
点评 本题考查盐类的水解,为高频考点,侧重考查学生的分析能力,注意把握盐类水解的原理,区别电离和水解,难度不大.

练习册系列答案
相关题目
15.下列实验过程始终无明显现象的是( )
| A. | CO2气体通入Ba(NO3)2溶液中 | B. | NO2气体通入FeSO4溶液中 | ||
| C. | H2S气体通入CuSO4溶液中 | D. | HC1气体通入NaSiO3溶液中 |
16.下列反应中,既属于氧化还原反应又属于置换反应的是( )
| A. | CuO+H2$\frac{\underline{\;高温\;}}{\;}$Cu+H2O | B. | CO2+Ca(OH)2═CaCO3↓+H2O | ||
| C. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2 | D. | 2Na+Cl2═2NaCl |
13.下列装置中,能构成原电池的是( )
| A. | 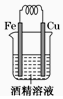 | B. | 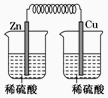 | C. | 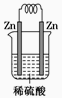 | D. | 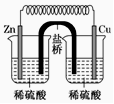 |
20.下列离子方程式书写正确的是( )
| A. | 氯气通入水中:Cl2+H2O═H++Cl-+HClO | |
| B. | 往AlCl3溶液中滴加稀NH3•H2O:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | Na2O2投入水中:2O22-+2H2O═4OH-+O2↑ | |
| D. | 向NaHCO3溶液中加过量Ca(OH)2溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O |
10.下列有关实验操作的解释或结论正确的是( )
| 选项 | 实验操作 | 解释或结论 |
| A | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色 | Fe(OH)3的溶解度小于Mg(OH)2的 |
| B | 用蒸馏水润湿的pH试纸测溶液的pH | 一定会使测定结果偏低 |
| C | 测定中和热时,使用碎泡沫起隔热保温的作用,用普通玻璃棒进行搅拌使酸和碱充分反应,准确读取实验时的最高温度并且取2~3次的实验平均值等,以达到良好的实验效果 | 用简易量热计测定反应热 |
| D | 用氢氧化钾与浓硫酸测定中和反应的反应热 | 测得的结果偏小 |
| A. | A | B. | B | C. | C | D. | D |
17.下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向两份蛋白质溶液中分别滴加饱和 NaCl液和 CuSO4 溶液 | 均有固体析出 | 蛋白质均发生变性 |
| B | 向溶液 X 中 先 滴 加 稀 硝 酸,再 滴 加Ba(NO3)2 溶液 | 出现白色沉淀 | 溶液 X 中不一定含有 SO42- |
| C | 灼烧白色粉末 | 火焰呈黄色 | 证明原粉末中有 Na +,无 K+ |
| D | 将溴水加入苯中 | 溴水颜色变浅 | 苯与溴水发生取代反应 |
| A. | A | B. | B | C. | C | D. | D |
9.下列变化过程,属于放热过程的是( )
①液态水变成水蒸气 ②酸碱中和反应 ③浓硫酸稀释
④固体氢氧化钠溶于水 ⑤H2在Cl2中燃烧
⑥NH4Cl晶体与Ba(OH)2•8H2O混合搅拌.
①液态水变成水蒸气 ②酸碱中和反应 ③浓硫酸稀释
④固体氢氧化钠溶于水 ⑤H2在Cl2中燃烧
⑥NH4Cl晶体与Ba(OH)2•8H2O混合搅拌.
| A. | ①⑤⑥ | B. | ②③④⑤ | C. | ②③④ | D. | ①③⑤ |
10.NA为阿伏加德罗常数,下列叙述错误的是( )
| A. | 18g H2O中含有的质子数为10NA | |
| B. | 25℃、101 kPa下,16 g O3和O2混合气体中含有的氧原子数为NA | |
| C. | 2.24LCO2中含有的原子数为0.3 NA | |
| D. | 1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |