题目内容
8.下列化学用语或元素性质说法正确的是( )| A. | 原子核外电子排布式为1s2的元素与原子核外电子排布式为1s22s2的元素化学性质相似 | |
| B. | NaCl的电子式: | |
| C. | F+的结构示意图: | |
| D. | Fe3+的最外层电子排布式为3s23p63d5 |
分析 A.1s2是He元素属于0族元素,1s22s2是Be元素属于第IIA族元素;
B.NaCl是离子化合物,由Na+、Cl-组成,电子式中需要标出电荷;
C.氟原子的核电荷数=9;
D.根据元素符号,判断元素原子的核外电子数,再根据核外电子排布规律来写.
解答 解:A.1s2是He元素属于0族元素,1s22s2是Be元素属于第IIA族元素,二者性质不同,故A错误;
B.氯化钠属于离子化合物,其电子式中需要标出阴阳离子所带电荷,氯化钠正确的电子式为: ,故B错误;
,故B错误;
C.氟离子核内质子数为9,核外电子数为10,其原子结构示意图为: ,故C错误;
,故C错误;
D.铁原子失去最外层4s能级2个电子,然后失去3d能级上的1个电子形成Fe3+,核外电子排布式为:1s22s22p63s23p63d5,故D正确.
故选D.
点评 本题考查了基态原子的核外电子排布式、电子式、离子结构示意图以及最外层的电子排布图,注意电子处于全满、半满、全空时最稳定,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.下列有关胶体及其性质的叙述正确的是( )
| A. | Fe(OH)3胶体无色、透明,能发生丁达尔现象 | |
| B. | 水泥厂、冶金厂常用高压电除去烟尘,是因为烟尘微粒带电荷 | |
| C. | 胶体与其它分散系的本质区别是胶体有丁达尔效应,而其它分散系却没有 | |
| D. | 纳米材料 微粒直径从几纳米到几十纳米(1nm=10-9m),因此纳米材料属于胶体 |
16.现有常温下pH=2的盐酸甲和pH=2的醋酸溶液乙,请根据下列操作回答问题:
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(2)取10mL的乙溶液,加入等体积的水,醋酸的电离平衡向右(填“向左”、“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中c(H+)/c(CH3COOH)的比值将减小(填“增大”、“减小”或“无法确定”).
(3)相同条件下,取等体积的甲、乙两溶液,各稀释100倍.稀释后的溶液,其pH大小关系为:pH(甲)>pH(乙)( 填“>”、“<”或“=”).
(4)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)< V(乙)( 填“>”、“<”或“=”).
(5)已知25℃时,两种酸的电离平衡常数如下:
下列四种离子结合H+能力最强的是B.
A.HCO3- B.CO32- C.ClO- D.CH3COO-
写出下列反应的离子方程式:CH3COOH+Na2CO3(少量):2CH3COOH+CO32-=H2O+2CH3COO-+CO2↑;HClO+Na2CO3(少量):HClO+CO32-=ClO-+HCO3-.
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(2)取10mL的乙溶液,加入等体积的水,醋酸的电离平衡向右(填“向左”、“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中c(H+)/c(CH3COOH)的比值将减小(填“增大”、“减小”或“无法确定”).
(3)相同条件下,取等体积的甲、乙两溶液,各稀释100倍.稀释后的溶液,其pH大小关系为:pH(甲)>pH(乙)( 填“>”、“<”或“=”).
(4)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)< V(乙)( 填“>”、“<”或“=”).
(5)已知25℃时,两种酸的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K1 | 1.8×10-5 | 4.3×10-7 | 3.0×10-8 |
| K2 | -- | 5.6×10-11 | -- |
A.HCO3- B.CO32- C.ClO- D.CH3COO-
写出下列反应的离子方程式:CH3COOH+Na2CO3(少量):2CH3COOH+CO32-=H2O+2CH3COO-+CO2↑;HClO+Na2CO3(少量):HClO+CO32-=ClO-+HCO3-.
3.能在水溶液中大量共存的一组离子是( )
| A. | H+、Fe2+、I-、NO3- | B. | Al3+、AlO2-、SO42-、Cl- | ||
| C. | K+、Ag+、Ca2+、NO3- | D. | NH4+、Na+、OH-、MnO4- |
20.下列有关有机物的说法正确的是( )
| A. | 1mol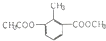 能与4molNaOH充分反应 能与4molNaOH充分反应 | |
| B. |  系统命名法为3-丁烯 系统命名法为3-丁烯 | |
| C. |  的碳原子都在一个平面内,且它的二氯代物为3种 的碳原子都在一个平面内,且它的二氯代物为3种 | |
| D. | 1mol 可以与4molH2发生加成 可以与4molH2发生加成 |
18.X、Y两元素可形成X2Y3型化合物,则X、Y原子基态时最外层的电子排布可能是( )
| A. | X:3s23p1 Y:3s23p5 | B. | X:2s22p2 Y:2s22p4 | ||
| C. | X:3s23p1 Y:3s23p4 | D. | X:3s2 Y:2s22p3 |
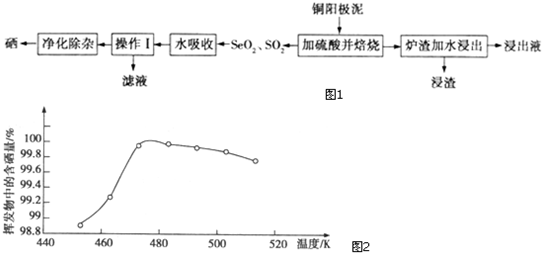
 某温度时,在1L密闭容器中,A、B、C三种气态物质的物质的量随时间变化的曲线如图所示.由图中数据分析:
某温度时,在1L密闭容器中,A、B、C三种气态物质的物质的量随时间变化的曲线如图所示.由图中数据分析: