题目内容
【题目】PbCrO4是一种黄色颜料,制备PbCrO4的一种实验步骤如下:
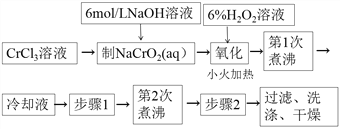
除图中标注的试剂外,实验中还用到6mol·L-1 醋酸,0.5 mol·L-1 Pb(NO3)2溶液,pH 试纸。
已知:①部分物质性质如下
物质 | 性质 | 颜色 | 溶解性 |
Cr(OH)3 | 两性氢氧化物 | 绿色 | 难溶于水 |
Pb(NO3)2 | - | 无色 | 易溶于水 |
Pb(CH3COO)2 | - | 无色 | 易溶于水 |
PbCrO4 | - | 黄色 | 难溶于水 |
Pb(OH)2 | 弱碱性 | 白色 | PH=7.2开始沉淀 ;PH=8.7完全沉淀 |
②PbCrO4可由沸腾的铬酸盐溶液与铅盐溶液作用制得,含PbCrO4晶种时更易生成
③六价铬在溶液中物种分布分数与pH关系如下图所示。
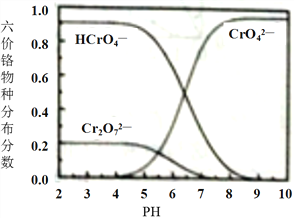
(1)“制NaCrO2(aq)”时,控制NaOH溶液加入量的操作方法是______。
(2)“氧化”时发生反应的离子方程式为______。
(3)下列说法正确的是(______)
A.两次煮沸的目的不相同
B.步骤2可以先加入一滴0.5mol·LPb(NO3)2溶液搅拌片刻,待产生少量沉淀后,继续滴加至有大量沉淀产生。
C.静置后,向上层清液中继续滴入Pb(NO3)2溶液,若无沉淀生成,则说明滴加完全。
D.小火加热的目的是为了避免反应过快。
(4)步骤1为__________________________________________________________。
(5)为测定产品的纯度,可用先用硝酸溶解PbCrO4,然后用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:Pb2+ + Y4- =PbY2-。测定时,先称取0.5000g无水PbCrO4产品,溶解后,用0.05000 mol·L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50 mL,则测得无水PbCrO4产品的纯度是_________(以质量分数表示)。
【答案】 不断搅拌下逐滴加入NaOH溶液,至产生的绿色沉淀恰好溶解 CrO2-+3H2O2+2OH-=2CrO42-+4H2O ABC 在不断搅拌下,向“冷却液”中加入6mol·L-1的醋酸至弱酸性(pH略小于7) 85.60%
【解析】(1)根据题给信息可知,Cr(OH)3为两性氢氧化物,溶于过量的强碱溶液,所以,制NaCrO2(aq)时,控制NaOH溶液加入量的操作方法是:不断搅拌下逐滴加入NaOH溶液,至产生的绿色沉淀恰好溶解为止;正确答案:不断搅拌下逐滴加入NaOH溶液,至产生的绿色沉淀恰好溶解。
(2)双氧水能够在碱性环境下,把+3价铬氧化为+6价铬,“氧化”时发生反应的离子方程式为CrO2-+3H2O2+2OH-=2CrO42-+4H2O;正确答案: CrO2-+3H2O2+2OH-=2CrO42-+4H2O。
(3)第一次煮沸是为了除去双氧水,第二次是把溶液浓缩,两次煮沸的目的不相同,A正确;将溶液加热至沸,先加入一滴0.5mol/LPb(NO3)2溶液搅拌片刻产生少量沉淀,然后继续滴加至有大量沉淀,步骤2可以先加入一滴0.5mol/LPb(NO3)2溶液搅拌片刻,待产生少量沉淀后,继续滴加至有大量沉淀PbCrO4产生,B正确;静置,向上层清液中滴入Pb(NO3)2溶液,若无沉淀生成,证明CrO42-沉淀完全,停止滴加,C正确;温度过高,双氧水易分解,D错误;正确选项ABC。
(4)由题意可知Pb2+在弱碱性环境下,生成Pb(OH)2沉淀,因此步骤1为目的就是提供弱酸性环境,具体操作为在不断搅拌下,向“冷却液”中加入6mol·L-1的醋酸至弱酸性(pH略小于7) ;正确答案: 在不断搅拌下,向“冷却液”中加入6mol·L-1的醋酸至弱酸性(pH略小于7) 。
(5)依据方程式Pb2+ + Y4- =PbY2-分析,PbCrO4的物质的量=0.0500mol/L×0.02650L=0.001325mol,PbCrO4的质量为0.001325mol×323=0.4280g,则则测得无水PbCrO4产品的纯度是0.4280/0.5000×100%=85.60%;正确答案:85.60%。

【题目】下列物质的分类中,所属关系不符合“X包含Y、Y包含Z”的有
选项 | X | Y | Z |
A | 芳香族化合物 | 芳香烃的衍生物 |
|
B | 脂肪族化合物 | 链状烃的衍生物 | CH3COOH(乙酸) |
C | 环状化合物 | 芳香族化合物 | 苯的同系物 |
D | 不饱和烃 | 芳香烃 |
|
A. A B. B C. C D. D
【题目】已知某化学实验的结果如下表:
实验序号 | 反应物 | 在相同温度下测得的反 | |
大小相同的金属片 | 酸溶液 | ||
1 | 镁条 | 1 mol·L-1盐酸 | v1 |
2 | 铁片 | 1 mol·L-1盐酸 | v2 |
3 | 铁片 | 0.1 mol·L-1盐酸 | v3 |
下列结论正确的是
A.v1>v2>v3B.v3>v2>v1C.v1>v3>v2D.v2>v3>v1


