题目内容
【题目】某种甲烷燃料电池采用铂作电极,电池中的质子交换膜只允许质子和水分子通过,其基本结构如图,电池总反应为:CH4+2O2═CO2+2H2O.下列有关说法正确的是( ) 
A.电子由a极流出经过负载流向b极
B.电解质溶液中H+移向a极
C.每转移1mole﹣ , 消耗1.6gCH4
D.b极上的电极反应式为:O2+2H2O+4e﹣=4OH﹣
【答案】A
【解析】解:A.通入燃料的电极为负极,所以a 是负极,通入氧化剂的电极为正极,所以b 是正极,则电子由a极流出经过负载流向b极,故A正确; B.b 是正极,电解质溶液中H+移向b极,故B错误;
C.a 是负极,电极反应式为CH4+2H2O﹣8e﹣═CO2+8H+ , 所以每转移1mole﹣ , 消耗2gCH4 , 故C错误;
D.b 是正极,正极上得电子发生还原反应,电极反应式为O2+4H++4e﹣═2H2O,故D错误;
故选A.

 名校课堂系列答案
名校课堂系列答案【题目】利用如图所示装置,采用适当试剂可完成下表的探究实验,并得出相应的实验结论,其中错误的是
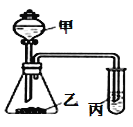
选项 | 甲 | 乙 | __丙 | 装置丙中的现象 | 实验结论 |
A | 稀硝酸 | 碳酸钾 | 澄淸石灰水 | 变浑浊 | 酸性:HNO3>H2CO3 |
B | 稀硫酸 | 碳酸钠 | 次氯酸钙溶液 | 白色沉淀 | 酸性:H2CO3>HClO |
C | 浓盐酸 | 大理石 | 硅酸钠溶液 | 白色沉淀 | 非金属性:C>Si |
D | 浓盐酸 | 高锰酸钾 | 石蕊溶液 | 先变红后褪色 | 氯水既有酸性,又具有漂白性 |
A. A B. B C. C D. D
【题目】在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10﹣5 |
下列说法不正确的是( )
A.上述生成Ni(CO)4(g)的反应为放热反应
B.25℃时反应Ni(CO)4(g)Ni(s)+4CO(g)的平衡常数为2×10﹣5
C.80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2 mol/L
D.在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol/L,则此时v(正)>v(逆)