题目内容
18.设NA为阿伏加德罗常数的数值.下列说法正确的是( )| A. | 标准状况下,11.2L苯中含有的碳碳双键数目为1.5NA | |
| B. | 常温常压下,2.8g由N2和CO组成的混合气体中含有的原子数为0.1NA | |
| C. | 25℃时,1.0LpH=12的Na2CO3溶液中含有的阴离子数大于0.01NA | |
| D. | 在反应:Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2中,生成1molCu,转移的电子数为2NA |
分析 A、苯不是单双键交替的结构;
B、氮气和CO的摩尔质量均为28g/mol,且均为双原子分子;
C、pH=12的Na2CO3溶液中氢氧根的浓度为0.01mol/L;
D、反应Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2转移6mol电子,生成2mol铜.
解答 解:A、苯不是单双键交替的结构,故结构中无碳碳双键,故A错误;
B、氮气和CO的摩尔质量均为28g/mol,且均为双原子分子,故2.8g混合物的物质的量为0.1mol,含0.2mol原子即0.2NA个,故B错误;
C、pH=12的Na2CO3溶液中氢氧根的浓度为0.01mol/L,故溶液中氢氧根的个数为0.01NA个,但溶液中含有碳酸根和碳酸氢根等阴离子,故阴离子的个数大于0.01NA个,故C正确;
D、反应Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2转移6mol电子,生成2mol铜,故当生成1mol铜时,转移3mol电子即3NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
1.在密闭容器中充入4mol HI,在一定温度下2HI(g)?H2(g)+I2(g)达到平衡时,有30%的HI发生分解,则平衡时混合气体总的物质的量是( )
| A. | 4 mol | B. | 3.4 mol | C. | 2.8 mol | D. | 1.2 mol |
6. 某兴趣活动小组利用物质间的互变,设计成一个平面魔方,如图所示:
某兴趣活动小组利用物质间的互变,设计成一个平面魔方,如图所示:
已知①A、B、C、D、G含有同种元素.
②
③E是通常情况下密度最小的气体;B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀,也能将一种氧化物氧化为F,F是含有三种元素的化合物,与A反应生成E、G.
依据以上信息填空:
(1)写出D的化学式:Fe2O3.
(2)G生成C的过程中所出现的现象为先产生白色沉淀,逐渐变为灰绿色,最后变为红褐色,写出该变化的化学方程式FeSO4+NaOH=Fe(OH)2↓+Na2SO4、4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(3)写出反应A转化为B的化学方程式:2Fe+3Cl2=2FeCl3.
(4)B→F的离子方程式为2Fe3++SO2+2H2O═2Fe2++SO42-+4H+.如何检验该反应生成的金属阳离子,简述操作方法及现象取反应后溶液少量滴入酸性高锰酸钾,若紫红色褪去,或滴入铁氰化钾生成蓝色沉淀即证明生成Fe2+离子.
 某兴趣活动小组利用物质间的互变,设计成一个平面魔方,如图所示:
某兴趣活动小组利用物质间的互变,设计成一个平面魔方,如图所示:已知①A、B、C、D、G含有同种元素.
②
| 纯A(单质) | B溶液 | D固体 | G溶液 | |
| 颜色 | 银白色 | 棕黄色 | 红棕色 | 浅绿色 |
依据以上信息填空:
(1)写出D的化学式:Fe2O3.
(2)G生成C的过程中所出现的现象为先产生白色沉淀,逐渐变为灰绿色,最后变为红褐色,写出该变化的化学方程式FeSO4+NaOH=Fe(OH)2↓+Na2SO4、4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(3)写出反应A转化为B的化学方程式:2Fe+3Cl2=2FeCl3.
(4)B→F的离子方程式为2Fe3++SO2+2H2O═2Fe2++SO42-+4H+.如何检验该反应生成的金属阳离子,简述操作方法及现象取反应后溶液少量滴入酸性高锰酸钾,若紫红色褪去,或滴入铁氰化钾生成蓝色沉淀即证明生成Fe2+离子.

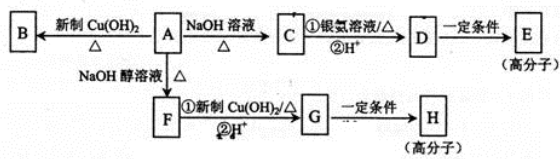
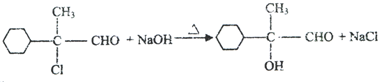 .
.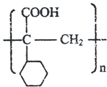 ,E的结构简式是
,E的结构简式是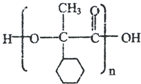 .
. 钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为:2Mn2++5S2O82-+8H2O$\frac{\underline{\;Ag+\;}}{\;}$2MnO4-+10SO42-+16H+
钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为:2Mn2++5S2O82-+8H2O$\frac{\underline{\;Ag+\;}}{\;}$2MnO4-+10SO42-+16H+