题目内容
7.依据:2Fe2++Cl2═2Fe3++2Cl-、2Fe3++Cu═2Fe2++Cu2+、Fe+Cu2+═Fe2++Cu,判断氧化性强弱顺序正确的是( )| A. | Fe3+>Cl2>Fe2+>Cu2+ | B. | Cl2>Fe3+>Cu2+>Fe2+ | ||
| C. | Cl2>Fe3+>Fe2+>Cu2+ | D. | Fe3+>Cl2>Cu2+>Fe2+ |
分析 在同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于还原产物的还原性,据此分析解答.
解答 解:2Fe2++Cl2=2Fe3++2Cl-中氯气是氧化剂,铁离子是氧化产物,所以氧化性Cl2>Fe3+;
2Fe3++Cu=Cu2++2Fe2+中铁离子是氧化剂,铜离子是氧化产物,所以氧化性Fe3+>Cu2+;
Fe+Cu2+=Fe2++Cu中铜离子是氧化剂,亚铁离子是氧化产物,所以氧化性Cu2+>Fe2+;
综上可得氧化剂的氧化性强弱顺序是Cl2>Fe3+>Cu2+>Fe2+;
故选B.
点评 本题考查氧化性强弱的判断,根据元素化合价变化来分析判断即可,注意规律的使用,难度不大.

练习册系列答案
相关题目
17.元素A的阳离子与元素B的阴离子具有相同的电子层结构.以下关于A、B元素的比较中,不正确的是( )
| A. | 原子半径:A<B | B. | 原子序数:A>B | ||
| C. | 原子最外层电子数:B>A | D. | 元素所在的周期数:A>B |
18.欲将NaCl、沙子(主要成份SiO2)、I2晶体的混合物分离,最科学的操作顺序是( )
| A. | 溶解、结晶、过滤、升华 | B. | 加热(升华)、溶解、过滤、蒸发(结晶) | ||
| C. | 加热(升华)、溶解、蒸馏、结晶 | D. | 溶解、过滤、加热(升华)、蒸发(结晶) |
15.下列名称都指同一物质的是( )
| A. | 胆矾、绿矾 | B. | 苏打、小苏打 | C. | 生石灰、碱石灰 | D. | 烧碱、苛性钠 |
2.下列根据实验现象所得出的结论中,一定正确的是( )
| 选项 | 实验现象 | 结论 |
| A | 无色试液中加入AgNO3溶液产生白色沉淀 | 试液中含有Cl- |
| B | 无色溶液加酚酞变红色 | 溶液的溶质是碱 |
| C | 碱性无色溶液中加入Na2CO3溶液产生白色沉淀 | 溶液中有Ca(OH)2 |
| D | 某气体能使湿润的红色石蕊试纸变蓝色 | 该气体中有NH3 |
| A. | A | B. | B | C. | C | D. | D |
12.实验室里用下列仪器和药品制取纯净的无水氯化铜.根据要求填写下列空白:
(1)如果按气体从左向右流时,②在④左边时,则②中加入液体的名称是饱和食盐水(填名称).
(2)装置⑥中发生反应的化学方程式是Cl2+2NaOH=NaCl+NaClO+H2O.
(3)实验开始时,应先点燃⑤(填装置序号)处的酒精灯,否则CuCl2中含有CuO(填化学式)杂质.待充分反应后,装置①的玻离管中剩余物呈棕黄色.冷却后,将制得的产物配成饱和溶液,溶液呈绿色.
(4)某小组推理反应结束后,⑤中一定有HCl剩余,请设计实验判断这一结论是否正确?加碳酸钠有气泡.
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 仪器及装置图 |  |  |  |  |  |  |
(2)装置⑥中发生反应的化学方程式是Cl2+2NaOH=NaCl+NaClO+H2O.
(3)实验开始时,应先点燃⑤(填装置序号)处的酒精灯,否则CuCl2中含有CuO(填化学式)杂质.待充分反应后,装置①的玻离管中剩余物呈棕黄色.冷却后,将制得的产物配成饱和溶液,溶液呈绿色.
(4)某小组推理反应结束后,⑤中一定有HCl剩余,请设计实验判断这一结论是否正确?加碳酸钠有气泡.
19.下列说法不正确的是( )
| A. | 乙烯、乙醇均能使酸性高锰酸钾溶液褪色 | |
| B. | 通过乙烷的取代反应或乙烯的加成反应都可以制取纯净的氯乙烷 | |
| C. | 乙烯、环己烷都属于烃类,它们通式相同,但它们不互为同系物 | |
| D. | 烯烃完全燃烧时,生成CO2和H2O的物质的量相等 |
17.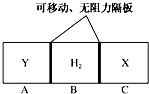 如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在C、A处充入均为10g的X、Y两种气体,且测得二者的密度相等.当隔板停止滑动时,下列说法一定正确的是( )
如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在C、A处充入均为10g的X、Y两种气体,且测得二者的密度相等.当隔板停止滑动时,下列说法一定正确的是( )
 如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在C、A处充入均为10g的X、Y两种气体,且测得二者的密度相等.当隔板停止滑动时,下列说法一定正确的是( )
如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在C、A处充入均为10g的X、Y两种气体,且测得二者的密度相等.当隔板停止滑动时,下列说法一定正确的是( )| A. | X、Y均为气体单质 | |
| B. | X、Y的相对分子质量相等 | |
| C. | n(H2)<n(X)=n(Y) | |
| D. | 隔板停止滑动时,A、B、C三部分体积相等 |