题目内容
3.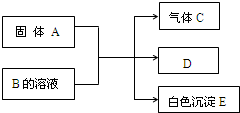 A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示,其中A是短周期中原子半径最大的元素构成的单质,E既可溶于盐酸又可溶于NaOH溶液.
A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示,其中A是短周期中原子半径最大的元素构成的单质,E既可溶于盐酸又可溶于NaOH溶液.(1)组成A的元素在周期表中的位置是3周期IA族.
(2)A的最高价氧化物对应水化物的电子式是
 .
.(3)E溶于NaOH溶液的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
(4)工业上冶炼A的化学反应中,若转移6mole-,可以得到的A的物质的量是6mol.
分析 A是短周期原子半径最大的元素(稀有气体除外)构成的单质,为Na,固体A与B反应生成白色沉淀E既可溶于盐酸又可溶于NaOH溶液,则E是Al(OH)3,则B应为AlCl3,气体C为H2,D应为NaCl,据此答题;
解答 解:A是短周期原子半径最大的元素(稀有气体除外)构成的单质,为Na,固体A与B反应生成白色沉淀E既可溶于盐酸又可溶于NaOH溶液,则E是Al(OH)3,则B应为AlCl3,气体C为H2,D应为NaCl,
(1)A为Na,在周期表中的位置是第3周期IA族,
故答案为:3周期IA族;
(2)A的最高价氧化物对应水化物为NaOH,其电子式是 ,
,
故答案为: ;
;
(3)Al(OH)3溶于NaOH溶液的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)Na是活泼金属,工业上冶炼A的化学反应为:2NaCl$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑,每转移1mol电子可得1molNa,所以转移6mole-,可以得到的A的物质的量是6mol,
故答案为:6 mol;
点评 本题考查无机物推断,明确物质的性质是解本题关键,熟练掌握常见元素化合物结构、性质,知道盐类水解特点,题目难度不大.

练习册系列答案
相关题目
13.下列电子式书写错误的是( )
| A. |  | B. | N??N | C. |  | D. | 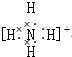 |
14.下列含氧酸中,酸性最弱的是( )
| A. | HClO | B. | HNO2 | C. | H2SO4 | D. | HIO4 |
11.下列选项中依次为:主要成分、杂质、除杂试剂或方法.其中排列顺序正确的是( )
| A. | 苯、苯酚、酒精灯 | B. | 乙烷、乙烯、溴水 | ||
| C. | 乙醇、水、金属钠 | D. | 苯、环己烷、高锰酸钾溶液 |
18.下列离子方程式正确的是( )
| A. | 稀硫酸加入氢氧化钡溶液中:H++OH-=H2O | |
| B. | 铜片上滴加稀硝酸:3Cu+8H++2 NO3-═3Cu2++2NO↑+4H2O | |
| C. | 石灰石投入到稀盐酸中:CO32-+2 H+=CO2↑+H2O | |
| D. | Fe 粉加入稀盐酸中:2 Fe+6 H+=2 Fe3++3 H2↑ |
8.下列分子或离子在指定的分散系中能大量共存的一组是( )
| A. | 银氨溶液:Na+、K+、NO3-、NH3•H2O | B. | 空气:C2H2、CO2、SO2、苯酚 | ||
| C. | 氢氧化铁胶体:H+、K+、S2-、Br- | D. | 高锰酸钾溶液:H+、Na+、SO42-、乙醇 |
12.下列物质属于烃类的是( )
| A. | 四氟乙烯 | B. | 碳酸 | C. | 氯仿 | D. | 十六烷 |
13.人们在生产和生活中认识到,几乎在所有的化学变化过程中都伴随着能量变化,例如放热、吸热、发光、放电等等.如果从能量变化的角度来认识,下面说法中正确的是( )
| A. | 化学变化都是吸热的 | |
| B. | 化学变化都是放热的 | |
| C. | 化学反应前后反应物和生成物所含能量会发生变化 | |
| D. | 反应物所含能量等于生成物所含能量 |
 ,乙炔的电子式为
,乙炔的电子式为
 的名称是3,3,4-三甲基己烷;
的名称是3,3,4-三甲基己烷; CH2=CH-CO18OCH2CH3+H2O.
CH2=CH-CO18OCH2CH3+H2O.