题目内容
9.钠和铝是两种重要的金属.请回答下列问题:(1)一小块金属钠放置在空气中,观察到的现象是①(填序号,下同);若金属钠常时间在潮湿的空气中放置,最后生成的物质是③.
①.金属表面逐渐失去金属光泽 ②.氢氧化钠 ③.碳酸钠
(2)将一小块金属钠投入水中,观察到的实验现象是②③(填序号),发生反应的离子方程式为2Na+2H2O═2Na++2OH-+H2↑.
①.钠沉到水底 ②.钠熔成小球 ③.小球四处游动
(3)铝是一种比较活泼的金属,在空气中极易被氧化而生成一种致密的氧化膜,从而保护内部的铝不再被氧化.请写出此反应的化学方程式4Al+3O2═2Al2O3.
分析 (1)切开金属钠置于空气中,切口开始呈银白色(钠的真面目)→变暗(生成Na2O)→变白色固体(生成NaOH)→成液(NaOH潮解)→结块(吸收CO2成Na2CO3•10H2O)→最后变成Na2CO3粉(风化);
(2)依据钠的物理性质及钠与水反应产物解答;
(3)铝易与氧气反应生成氧化铝.
解答 解:(1)钠性质活泼,易与氧气反应,切开金属钠置于空气中,切口开始呈银白色→变暗→变白色固体→成液→结块→最后变成Na2CO3粉末,
故答案为:①;③;
(2)钠密度小于水,熔点低,浮在水面,钠与水反应生成氢氧化钠和氢气,方程式:2Na+2H2O=2Na++2OH-+H2↑,反应放热,使钠熔化成小球,产生的 氢气推动钠四处游动,
故答案为:②③;2Na+2H2O═2 Na++2OH-+H2↑;
(3)铝易与氧气反应生成氧化铝,方程式为4Al+3 O2═2Al2O3,故答案为:4Al+3 O2═2Al2O3.
点评 本题综合考查元素化合物知识,为高频考点,侧重考查学生的分析能力以及元素化合物知识的综合理解和运用,注意把握物质的性质以及反应现象的判断,难度不大.

练习册系列答案
相关题目
4.关于 的分子结构说法正确的是( )
的分子结构说法正确的是( )
 的分子结构说法正确的是( )
的分子结构说法正确的是( )| A. | 分子中12个碳原子一定在同一平面 | |
| B. | 分子中有7个碳原子可能在同一直线上 | |
| C. | 分子中最多有6个碳原子能在同一直线上 | |
| D. | 分子中最多有8个碳原子能在同一直线上 |
1.下列关于热化学反应的描述正确的是( )
| A. | CO 的燃烧热是 283.0 KJ/mol,则2CO2(g)=2CO(g)+O2(g)△H=+283.0 KJ/mol | |
| B. | HC1和NaOH反应的中和热△H=-57.3 KJ/mol,则H2SO4和Ba(OH)2的反应热△H=2×(-57.3)KJ/mol | |
| C. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量少 | |
| D. | 已知:H-H键的键能为a KJ/mol,Cl-C1键的键能为b KJ/mol,H-C1键的键能为c KJ/mol,则生成1 mol HC1放出的能量为$\frac{(a+b-2c)}{2}$KJ |

 +3Br2→
+3Br2→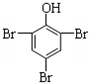 ↓+3HBr;反应类型取代反应.
↓+3HBr;反应类型取代反应. ;反应类型取代反应.
;反应类型取代反应. ;反应类型加聚反应.
;反应类型加聚反应. ;HCN的结构式是H-C≡N;
;HCN的结构式是H-C≡N; ;
; 所含官能团的名称是碳碳双键,醛基;该有机物发生加聚反应后,所得产物的结构简式为
所含官能团的名称是碳碳双键,醛基;该有机物发生加聚反应后,所得产物的结构简式为 .
.