题目内容
5.某化合物的性质如下:①加入氢氧化钠溶液,加热,产生使湿润的红色石蕊试纸变蓝的气体;②溶于水,加入硝酸钡溶液,产生能溶于稀硝酸的白色沉淀.则该物质是( )| A. | NH4Cl | B. | (NH4)2CO3 | C. | NaCl | D. | K2SO4 |
分析 能使湿润的红色石蕊试纸变蓝色的气体是氨气;该物质的溶液能和硝酸钡反应产生能溶于稀硝酸的白色沉淀,说明该物质中的阴离子为弱酸根离子,以此解答该题.
解答 解:能使湿润的红色石蕊试纸变蓝色的气体是氨气,该化合物和氢氧化钠溶液反应生成氨气,说明该物质中含有铵根离子;
该物质的溶液能和硝酸钡反应产生能溶于稀硝酸的白色沉淀,说明该物质中的阴离子为弱酸根离子,但不能为亚硫酸根离子;
A.在加热条件下,氯化铵能和强碱反应生成氨气,但和硝酸钡不反应,故A错误;
B.在加热条件下,碳酸铵和强碱反应生成氨气,和硝酸钡反应生成碳酸钡沉淀,但碳酸钡能溶于稀硝酸,故B正确;
C.氯化钠和氢氧化钠不反应,故C错误;
D.硫酸钾和氢氧化钠不反应,故D错误;
故选B.
点评 本题考查了物质的推断,根据氨气的性质确定铵根离子、根据沉淀的性质确定碳酸根离子,从而确定该化合物的构成,注意亚硫酸钡能被硝酸氧化生成硫酸钡,为易错点.

练习册系列答案
相关题目
15.下列有机物:①CH3OH ②CH3CH2OH ③CH3CHOHCH2CH3 ④(CH3)2CHCH2OH⑤HOCH2CH(CH3)2⑥(CH3)3COH下列判断正确的是( )
| A. | ①②③④⑤⑥之间的关系为同系物 | B. | ③⑥不是同分异构体 | ||
| C. | 可发生消去反应的有机物有4 | D. | 能被催化氧化为醛的有机物有4种 |
13.下列说法错误的是( )
| A. | 主族元素的最外层电子数都等于它的最高正化合价 | |
| B. | 同一主族的元素的原子最外层电子数相等 | |
| C. | 同周期的主族元素随核电荷数的递增原子半径逐渐减小 | |
| D. | 第N周期有N种主族元素是金属元素(N>1) |
20.某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理.
(1)请写出SO2与过量NaOH溶液反应的离子方程式:SO2+2OH-=SO32-+H2O.
(2)吸收尾气(Cl2)一段时间后,吸收液(强碱性)中肯定存在的阴离子有OH-和Cl-、SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响)
①提出合理假设.
假设1:只存在SO32-;
假设2:既不存在SO32-也不存在ClO-;
假设3:只存在ClO-.
②要证明假设1是否成立,设计实验方案,进行实验.请在答题卡上写出实验以及预期现象和结论.限选实验试剂:3mol•L-1H2SO4、1mol•L-1NaOH、0.01mol•L-1KMnO4、淀粉-KI溶液.
(1)请写出SO2与过量NaOH溶液反应的离子方程式:SO2+2OH-=SO32-+H2O.
(2)吸收尾气(Cl2)一段时间后,吸收液(强碱性)中肯定存在的阴离子有OH-和Cl-、SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响)
①提出合理假设.
假设1:只存在SO32-;
假设2:既不存在SO32-也不存在ClO-;
假设3:只存在ClO-.
②要证明假设1是否成立,设计实验方案,进行实验.请在答题卡上写出实验以及预期现象和结论.限选实验试剂:3mol•L-1H2SO4、1mol•L-1NaOH、0.01mol•L-1KMnO4、淀粉-KI溶液.
| 实验 | 预期现象和结论 |
在试管加少量的吸收液,再滴加0.01mol•L-1KMnO4溶液 | 若紫红色褪去,证明有SO32-,则说明假设1成立,否则假设1不成立 |
10.下列有关胶体的说法中,不正确的是( )
| A. | 胶体、溶液、浊液的分类依据是分散质微粒直径大小 | |
| B. | “卤水点豆腐”、“黄河入海口处的沙洲”都与胶体的聚沉有关 | |
| C. | 向1 mol•L-1氯化铁溶液中加入少量的NaOH溶液制取氢氧化铁胶体 | |
| D. | 可以用丁达尔现象区别硫酸铜溶液和氢氧化铁胶体 |
17.已知可逆反应2SO2+O2 $?_{△}^{催化剂}$2SO3,当生成2mol SO3时放出热量为Q,现将1mol SO2和0.5mol O2在相同条件下反应生成SO3放出的热量为Q1,则( )
| A. | Q1=Q | B. | Q1<Q | C. | 2Q1<Q | D. | 无法判断 |
14.下列说法中正确的是( )
| A. | 纯净物中一定存在化学键 | |
| B. | 阴、阳离子间通过静电引力而形成的化学键叫做离子键 | |
| C. | 只有金属元素和非金属元素化合时才能形成离子键 | |
| D. | 离子化合物中可能含共价键,共价化合物中不含离子键 |
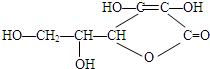 有机化合物的化学性质本质上就是分子结构中所含官能团的性质:
有机化合物的化学性质本质上就是分子结构中所含官能团的性质: ;
;