��Ŀ����
��֪0.1mol�л���A��������12g���������������г��ȼ�պ�����35.2g CO2��7.2g H2O�� A���Է���������Ӧ���䱽���ϵ�һ±���������֣�
��1��A�Ľṹ��ʽΪ______��

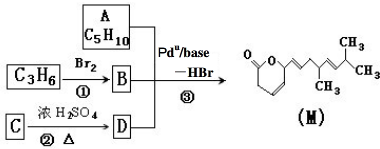
��������ת����ϵ��
����D��ʹ������Ȼ�̼��Һ��ɫ��F��������������G��G����Է�������Ϊ90��
��2��C���ܾ��еĻ�ѧ������______������ţ�
������H2�����ӳɷ�Ӧ �����ڼ�����Һ�з���ˮ�ⷴӦ
��������ᷢ��������Ӧ ������Ag��NH3��2OH��Һ����������Ӧ
��3��д�����з�Ӧ�Ļ�ѧ����ʽ���л����ýṹ��ʽ��ʾ������ָ���䷴Ӧ����
��Cת��ΪD�ķ�Ӧ______����Ӧ���ͣ�______��Ӧ��
��һ�������£�D���ɸ߷��ӻ�����ķ�Ӧ______����Ӧ���ͣ�______��Ӧ��
��4����ʢ��5mL G������Һ���Թ��е���3����ϡ�����ữ��KMnO4��Һ������Һ���Ϻ�ɫ��ȥ����֪MnO4-ת��ΪMn2+����÷�Ӧ�Ļ�ѧ����ʽΪ��______
��5��C��ͬ���칹���ж��֣����з�������Ҫ����л�����______��
����C������ͬ�Ĺ��������� �������Ȼ�����Һ����ɫ
�۱����ϵ�һ�ȴ���ֻ������
��д�����е�һ��ͬ���칹�壺______��
��1��A�Ľṹ��ʽΪ______��

��������ת����ϵ��
����D��ʹ������Ȼ�̼��Һ��ɫ��F��������������G��G����Է�������Ϊ90��
��2��C���ܾ��еĻ�ѧ������______������ţ�
������H2�����ӳɷ�Ӧ �����ڼ�����Һ�з���ˮ�ⷴӦ
��������ᷢ��������Ӧ ������Ag��NH3��2OH��Һ����������Ӧ
��3��д�����з�Ӧ�Ļ�ѧ����ʽ���л����ýṹ��ʽ��ʾ������ָ���䷴Ӧ����
��Cת��ΪD�ķ�Ӧ______����Ӧ���ͣ�______��Ӧ��
��һ�������£�D���ɸ߷��ӻ�����ķ�Ӧ______����Ӧ���ͣ�______��Ӧ��
��4����ʢ��5mL G������Һ���Թ��е���3����ϡ�����ữ��KMnO4��Һ������Һ���Ϻ�ɫ��ȥ����֪MnO4-ת��ΪMn2+����÷�Ӧ�Ļ�ѧ����ʽΪ��______
��5��C��ͬ���칹���ж��֣����з�������Ҫ����л�����______��
����C������ͬ�Ĺ��������� �������Ȼ�����Һ����ɫ
�۱����ϵ�һ�ȴ���ֻ������
��д�����е�һ��ͬ���칹�壺______��
35.2g CO2�����ʵ���Ϊ
=0.8mol��m��C��=0.8mol��12g/mol=9.6g��7.2g H2O�����ʵ���Ϊ
=0.4mol��m��H��=0.4mol��2��1g/mol=0.8g����12g���A��m��O��=12g-9.6g-0.8g=1.6g����n��O��=
=0.1mol�����л���A������Cԭ����ĿΪ
=8��Hԭ����ĿΪ
=8��Oԭ����ĿΪ
=1����A�ķ���ʽΪC8H8O���л���A���Է���������Ӧ�������к���-CHO�������ϵ�һ±���������֣�˵����������1��֧������AΪ
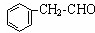
������Ϣ���֪��
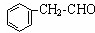
��HCN�����ӳɷ�Ӧ����B����BΪ
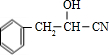
��Bˮ������C����CΪ
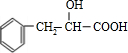
��C��Ũ���ᡢ��������������D��D��ʹ������Ȼ�̼��Һ��ɫ����Ϊ������ȥ��Ӧ����DΪ
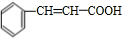
��
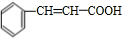
��������E��F������Ϣ���֪����Ϊ
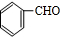
��OHC-COOH��F��������������G��G����Է�������Ϊ90����FΪOHC-COOH��EΪ

��GΪHOOC-COOH��
��1��������������֪��AΪ
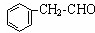
���ʴ�Ϊ��
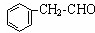
��
��2��C��
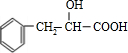
�����б��������������������ӳɷ�Ӧ�������ǻ�����������ᷢ��������Ӧ�������ڼ�����Һ�з���ˮ�ⷴӦ��������Ag��NH3��2OH��Һ����������Ӧ���ʴ�Ϊ���٢ۣ�
��3����
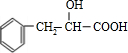
��Ũ���ᡢ���������·�����ȥ��Ӧ����
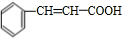
����Ӧ����ʽΪ��
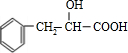
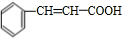
+H2O��
�ʴ�Ϊ��
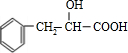
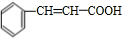
+H2O����ȥ��
��һ�������£�
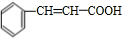
���ɸ߷��ӻ�����ķ�ӦΪ
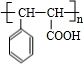
����Ӧ����ʽΪn
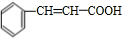

�����ڼӾ۷�Ӧ��
�ʴ�Ϊ��n
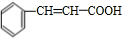

���Ӿۣ�
��4����ʢ��5mLHOOC-COOH������Һ���Թ��е���3����ϡ�����ữ��KMnO4��Һ������Һ���Ϻ�ɫ��ȥ��MnO4-ת��ΪMn2+��ͬʱ���ɶ�����̼��ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ��5H2C2O4+2KMnO4+3H2SO4=K2SO4+2MnSO4+10CO2��+8H2O���ʴ�Ϊ��5H2C2O4+2KMnO4+3H2SO4=K2SO4+2MnSO4+10CO2��+8H2O��
��5��
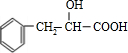
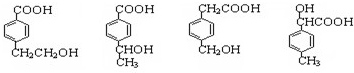
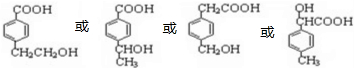
��ͬ���칹���ж��֣����з�������Ҫ�����C������ͬ�Ĺ��������࣬����-OH��-COOH���������Ȼ�����Һ����ɫ���������ǻ����۱����ϵ�һ�ȴ���ֻ�����֣�������Ϊ��λ��Ԫȡ��������ͬ���칹���У�
��
�ʴ�Ϊ��4��
��
| 35.2g |
| 44g/mol |
| 7.2g |
| 18g/mol |
| 1.6g |
| 16g/mol |
| 0.8mol |
| 0.1mol |
| 0.4mol��2 |
| 0.1mol |
| 0.1mol |
| 0.1mol |
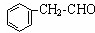
������Ϣ���֪��
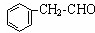
��HCN�����ӳɷ�Ӧ����B����BΪ
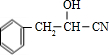
��Bˮ������C����CΪ
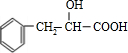
��C��Ũ���ᡢ��������������D��D��ʹ������Ȼ�̼��Һ��ɫ����Ϊ������ȥ��Ӧ����DΪ
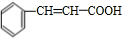
��
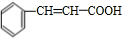
��������E��F������Ϣ���֪����Ϊ

��OHC-COOH��F��������������G��G����Է�������Ϊ90����FΪOHC-COOH��EΪ

��GΪHOOC-COOH��
��1��������������֪��AΪ
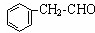
���ʴ�Ϊ��
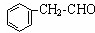
��
��2��C��
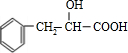
�����б��������������������ӳɷ�Ӧ�������ǻ�����������ᷢ��������Ӧ�������ڼ�����Һ�з���ˮ�ⷴӦ��������Ag��NH3��2OH��Һ����������Ӧ���ʴ�Ϊ���٢ۣ�
��3����
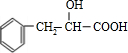
��Ũ���ᡢ���������·�����ȥ��Ӧ����
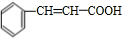
����Ӧ����ʽΪ��
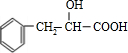
| Ũ���� |
| �� |
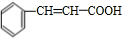
+H2O��
�ʴ�Ϊ��
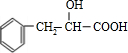
| Ũ���� |
| �� |
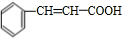
+H2O����ȥ��
��һ�������£�
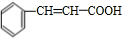
���ɸ߷��ӻ�����ķ�ӦΪ

����Ӧ����ʽΪn
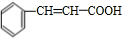
| һ������ |

�����ڼӾ۷�Ӧ��
�ʴ�Ϊ��n
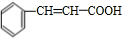
| һ������ |

���Ӿۣ�
��4����ʢ��5mLHOOC-COOH������Һ���Թ��е���3����ϡ�����ữ��KMnO4��Һ������Һ���Ϻ�ɫ��ȥ��MnO4-ת��ΪMn2+��ͬʱ���ɶ�����̼��ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ��5H2C2O4+2KMnO4+3H2SO4=K2SO4+2MnSO4+10CO2��+8H2O���ʴ�Ϊ��5H2C2O4+2KMnO4+3H2SO4=K2SO4+2MnSO4+10CO2��+8H2O��
��5��
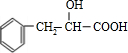
��ͬ���칹���ж��֣����з�������Ҫ�����C������ͬ�Ĺ��������࣬����-OH��-COOH���������Ȼ�����Һ����ɫ���������ǻ����۱����ϵ�һ�ȴ���ֻ�����֣�������Ϊ��λ��Ԫȡ��������ͬ���칹���У�

��
�ʴ�Ϊ��4��

��

��ϰ��ϵ�д�
 ��Уͨ��֤��Ч��ҵϵ�д�
��Уͨ��֤��Ч��ҵϵ�д�
�����Ŀ
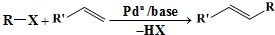 ��ش��������⣺
��ش��������⣺