题目内容
写出下列反应的化学方程式,并指出氧化剂和还原剂.
(1)锂在空气中燃烧
(2)钾与水反应
(3)镁条在二氧化碳气体中燃烧
(4)曾青得铁则化为铜--湿法炼铜
(5)从赤铁矿中提炼铁--工业冶铁 .
(1)锂在空气中燃烧
(2)钾与水反应
(3)镁条在二氧化碳气体中燃烧
(4)曾青得铁则化为铜--湿法炼铜
(5)从赤铁矿中提炼铁--工业冶铁
考点:化学方程式的书写,氧化还原反应
专题:化学用语专题,氧化还原反应专题
分析:(1)锂在空气中燃烧反应生成氧化锂,锂元素的化合价升高,氧元素的化合价降低;
(2)钾与水反应生成氢氧化钾和氢气,钾元素的化合价升高,氢元素的化合价降低;
(3)镁条在二氧化碳气体中燃烧生成氧化镁和碳,镁元素的化合价升高,碳元素的化合价降低;
(4)曾青得铁则化为铜--湿法炼铜为铁和硫酸铜发生置换反应生成硫酸亚铁和铜,铁元素的化合价升高,铜元素的化合价降低;
(5)从赤铁矿中提炼铁--工业冶铁为三氧化二铁和一氧化碳反应,反应生成铁和二氧化碳,碳元素的化合价升高,铁元素的化合价降低;
(2)钾与水反应生成氢氧化钾和氢气,钾元素的化合价升高,氢元素的化合价降低;
(3)镁条在二氧化碳气体中燃烧生成氧化镁和碳,镁元素的化合价升高,碳元素的化合价降低;
(4)曾青得铁则化为铜--湿法炼铜为铁和硫酸铜发生置换反应生成硫酸亚铁和铜,铁元素的化合价升高,铜元素的化合价降低;
(5)从赤铁矿中提炼铁--工业冶铁为三氧化二铁和一氧化碳反应,反应生成铁和二氧化碳,碳元素的化合价升高,铁元素的化合价降低;
解答:
解:(1)锂在空气中燃烧4Li+O2
2Li2O,反应中氧元素化合价从0价变化为-2价,化合价降低得到电子,所以O2做氧化剂,锂元素的化合价从0价变化为+1价,元素化合价升高失电子,所以Li做还原剂,
故答案为:4Li+O2
2Li2O;氧化剂:O2还原剂:Li;
(2)钾与水反应2K+2H2O=2KOH+H2↑,反应中氢元素化合价从+1价变化为0价,化合价降低得到电子,所以H2O做氧化剂,钾元素的化合价从0价变化为+1价,元素化合价升高失电子,所以K做还原剂,
故答案为:2K+2H2O=2KOH+H2↑;氧化剂:H2O还原剂:K;
(3)镁条在二氧化碳气体中燃烧2Mg+CO2
2MgO+C,反应中碳元素化合价从+4价变化为0价,化合价降低得到电子,所以CO2做氧化剂,镁元素的化合价从0价变化为+2价,元素化合价升高失电子,所以Mg做还原剂,
故答案为:2Mg+CO2
2MgO+C;氧化剂:CO2还原剂:Mg;
(4)曾青得铁则化为铜--湿法炼铜CuSO4+Fe=FeSO4+Cu,反应中铜元素化合价从+2价变化为0价,化合价降低得到电子,所以CuSO4做氧化剂,铁元素的化合价从0价变化为+2价,元素化合价升高失电子,所以铁做还原剂,
故答案为:CuSO4+Fe=FeSO4+Cu;氧化剂:CuSO4还原剂:Fe;
(5)从赤铁矿中提炼铁--工业冶铁Fe2O3+3CO
2Fe+3CO2,反应中铁元素化合价从+3价变化为0价,化合价降低得到电子,所以Fe2O3做氧化剂,碳元素的化合价从+2价变化为+4价,元素化合价升高失电子,所以CO做还原剂,
故答案为:Fe2O3+3CO
2Fe+3CO2;氧化剂:Fe2O3还原剂:CO;
| ||
故答案为:4Li+O2
| ||
(2)钾与水反应2K+2H2O=2KOH+H2↑,反应中氢元素化合价从+1价变化为0价,化合价降低得到电子,所以H2O做氧化剂,钾元素的化合价从0价变化为+1价,元素化合价升高失电子,所以K做还原剂,
故答案为:2K+2H2O=2KOH+H2↑;氧化剂:H2O还原剂:K;
(3)镁条在二氧化碳气体中燃烧2Mg+CO2
| ||
故答案为:2Mg+CO2
| ||
(4)曾青得铁则化为铜--湿法炼铜CuSO4+Fe=FeSO4+Cu,反应中铜元素化合价从+2价变化为0价,化合价降低得到电子,所以CuSO4做氧化剂,铁元素的化合价从0价变化为+2价,元素化合价升高失电子,所以铁做还原剂,
故答案为:CuSO4+Fe=FeSO4+Cu;氧化剂:CuSO4还原剂:Fe;
(5)从赤铁矿中提炼铁--工业冶铁Fe2O3+3CO
| ||
故答案为:Fe2O3+3CO
| ||
点评:本题考查化学反应及氧化还原反应中氧化剂、还原剂的判断,元素化合价的变化是氧化还原反应的判断依据和特征,依据化合价变化分析,“升失氧,降得还”,题目难度不大.

练习册系列答案
相关题目
下列关于胶体的叙述中,不正确的是( )
| A、向胶体中加入蔗糖溶液,产生聚沉现象 |
| B、可见光透过胶体时,发生丁达尔现象 |
| C、用渗析的方法“净化”胶体时,使用的半透膜只能让分子、离子通过 |
| D、胶体能吸附阳离子或阴离子,故在电场作用下会产生电泳现象 |
三种短周期元素A、B和C,它们的原子序数是依次增大,其中C的原子半径在短周期的主族元素中最大,B和C的最外层电子数之和等于A的最外层电子数的2倍,且A是构成有机物的重要元素,下列说法正确的是( )
| A、A元素位于元素周期表中第二周期ⅥA族 |
| B、B离子与C离子具有相同的电子层结构 |
| C、C离子具有很强的还原性,B离子具有很强的氧化性 |
| D、B、C可以形成BC2型化合物 |
 已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:
已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡: 与足量的NaOH溶液充分反应,消耗的NaOH的总的物质的量为
与足量的NaOH溶液充分反应,消耗的NaOH的总的物质的量为
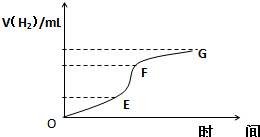 ( I)用纯净的锌粒与100mL2mol/L稀盐酸反应制取氢气,请回答:
( I)用纯净的锌粒与100mL2mol/L稀盐酸反应制取氢气,请回答: