题目内容
最近,科学家冶炼出了纯度高达99.9999%的铁,你估计它不会具有的性质是( )
| A、硬度比生铁低 |
| B、在潮湿的空气中放置不易生锈 |
| C、在冷的浓硫酸中钝化 |
| D、不能与盐酸反应 |
考点:金属与合金在性能上的主要差异
专题:几种重要的金属及其化合物
分析:A.生铁是合金,硬度大于纯铁;
B.铁在潮湿的空气中易生锈;
C.浓硫酸具有强的氧化性,低温下能够使铁发生钝化;
D.铁排在氢的前面,能够与盐酸反应生成氢气.
B.铁在潮湿的空气中易生锈;
C.浓硫酸具有强的氧化性,低温下能够使铁发生钝化;
D.铁排在氢的前面,能够与盐酸反应生成氢气.
解答:
解:A.生铁是合金,合金的硬度大,故A正确;
B.铁在有水和氧气并存时易生锈,故B正确;
C.铁能在冷的浓硫酸中可发生钝化而不溶解,故C正确;
D.铁排在氢的前面,能够与盐酸反应生成氢气,故D错误;
故选:D.
B.铁在有水和氧气并存时易生锈,故B正确;
C.铁能在冷的浓硫酸中可发生钝化而不溶解,故C正确;
D.铁排在氢的前面,能够与盐酸反应生成氢气,故D错误;
故选:D.
点评:本题考查铁与合金的性质,难度不大,注意铁在有水和氧气并存时易生锈.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
乙酸的分子结构为 ,下列关于反应与断键部位叙述正确的是( )
,下列关于反应与断键部位叙述正确的是( )
(1)乙酸与乙醇发生酯化反应时,②键断裂
(2)乙酸的电离以及与酸的通性有关的反应,是③键断裂
(3)在红磷存在时,Br2可与CH3COOH发生反应:Br2+CH3COOH
CH2Br-COOH+HBr,是③键断裂
(4)乙酸变成乙酸酐的反应:2CH3COOH→ +H2O,是①②键断裂.
+H2O,是①②键断裂.
 ,下列关于反应与断键部位叙述正确的是( )
,下列关于反应与断键部位叙述正确的是( )(1)乙酸与乙醇发生酯化反应时,②键断裂
(2)乙酸的电离以及与酸的通性有关的反应,是③键断裂
(3)在红磷存在时,Br2可与CH3COOH发生反应:Br2+CH3COOH
| 红磷 |
(4)乙酸变成乙酸酐的反应:2CH3COOH→
 +H2O,是①②键断裂.
+H2O,是①②键断裂.| A、(1)(2)(3) |
| B、(2)(3)(4) |
| C、(1)(3)(4) |
| D、(1)(2)(4) |
下列电离方程式错误的是( )
| A、NaHS溶于水:NaHS═Na++HS-,HS-+H2O?H3O++S2- | ||||||
B、Al(OH)3电离:H2O+AlO
| ||||||
C、(NH4)2SO4溶于水:(NH4)2SO4?2NH
| ||||||
| D、HF溶于水:HF+H2O?H3O++F- |
下列物质中不可能由一种元素组成的是( )
| A、单质 | B、氧化物 |
| C、化合物 | D、混合物 |
有关 的说法不正确的是( )
的说法不正确的是( )
 的说法不正确的是( )
的说法不正确的是( )| A、分子式为:C10H16 |
| B、所有原子可共面 |
| C、其环上的一氯代物为三种 |
| D、该物质以及加氢产物都不存在手性碳原子 |
将二氧化碳通入Ba(OH)2稀溶液中,能正确表示其导电能力变化的是( )
A、 |
B、 |
C、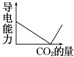 |
D、 |

