题目内容
8.图中每条折线表示周期表IVA~VIIA中的某一族元素氢化物的沸点变化,其中a点代表的是( )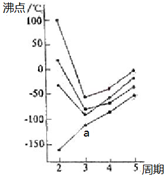
| A. | SiH4 | B. | HCl | C. | PH3 | D. | H2S |
分析 根据氢化物的相对分子质量越大,物质熔沸点越高,分子间含有氢键的熔沸点反常,据此分析.
解答 解:在ⅣA~ⅦA中的氢化物里,相对分子质量越大,物质熔沸点越高,NH3、H2O、HF因存在氢键,故沸点高于同主族相邻元素氢化物的沸点,只有ⅣA族元素氢化物不存在反常现象,故a点代表的应是SiH4.
故选A.
点评 本题考查了氢键的存在对物质性质的影响,侧重考查学生对一般规律中异常现象的辨别能力,题目难度不大.

练习册系列答案
相关题目
19.下列实验室制取气体的反应中,属于非离子反应,且生成的气体为非电解质的是( )
| A. | 实验室制取氯气 | B. | 实验室制取氧气 | ||
| C. | 实验室制取二氧化碳 | D. | 实验室制取氨气 |
16.分子式为C5H11Cl的有机化合物有( )
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
3.下列有关碱金属的叙述正确的是( )
| A. | 碱金属都可以保存在煤油中 | |
| B. | 碱金属在空气中燃烧都能生成M2O(M表示碱金属) | |
| C. | 随着原子序数的增加,碱金属的熔点降低 | |
| D. | 碱金属着火应用泡沫灭火剂更好 |
13.全世界每年因钢铁锈蚀造成大量的损失.某学生欲探究在蒸馏水、氯化钠溶液和醋酸溶液三种条件下铁锈蚀的快慢,设计了如下实验.
请回答:
(1)在一周的观察过程中,他发现实验序号为①的试管中铁钉锈蚀速度最慢.
(2)实验②中发生的是吸氧腐蚀(填“析氢腐蚀”或“吸氧腐蚀”),溶液显碱性(填“酸”、“碱”或“中”),用相关电极方程式解释2H2O+O2+4e-=4OH-
(3)下列防止钢铁锈蚀的措施合理的是ac(填字母).
a.在自行车的钢圈表面镀镍
b.在地下钢铁管道上连接铜块
c.改变金属内部结构制成不锈钢.
| 实验序号 | ① | ② | ③ |
| 实验 内容 |  |  |  |
(1)在一周的观察过程中,他发现实验序号为①的试管中铁钉锈蚀速度最慢.
(2)实验②中发生的是吸氧腐蚀(填“析氢腐蚀”或“吸氧腐蚀”),溶液显碱性(填“酸”、“碱”或“中”),用相关电极方程式解释2H2O+O2+4e-=4OH-
(3)下列防止钢铁锈蚀的措施合理的是ac(填字母).
a.在自行车的钢圈表面镀镍
b.在地下钢铁管道上连接铜块
c.改变金属内部结构制成不锈钢.
18.下列关于硅及其化合物的说法不正确的是( )
| A. | 单质硅常用作半导体材料 | |
| B. | 硅酸钠是制备木材防火剂的原料 | |
| C. | 二氧化硅是制备光导纤维的基本原料 | |
| D. | 硅酸可由二氧化硅与水直接反应制得 |
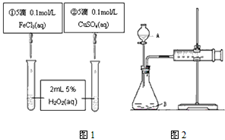 为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲乙两组同学分别设计了如图1、图2所示的实验.请回答下列问题
为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲乙两组同学分别设计了如图1、图2所示的实验.请回答下列问题
 .
.