题目内容
下列离子方程式不正确的是( )
| A、三氯化铝溶液中加入过量氨水:Al3++4NH3?H2O=AlO2-+2H2O+4NH4+ |
| B、4mol/L的NaAlO2溶液和7mol/L的HCl等体积互相均匀混合:4AlO2-+7H++H2O=3Al(OH)3↓+Al3+ |
| C、在Mn2+溶液中加入HNO3再加入PbO2得紫红色溶液:5PbO2+2Mn2++4H+=5Pb2++2MnO4-+2H2O |
| D、将0.1mol/L Na2CO3溶液数滴缓缓滴入O.1mol/L 25mL盐酸中2H++CO32-=CO2↑+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A、过量氨水不能溶解氢氧化铝沉淀;
B、4mol/L的NaAlO2溶液和7mol/L的HCL等体积,依据化学反应定量关系分析判断;
C、PbO2具有强氧化性氧化锰离子为高锰酸根离子;
D、碳酸钠滴入过量盐酸溶液中会反应生成二氧化碳.
B、4mol/L的NaAlO2溶液和7mol/L的HCL等体积,依据化学反应定量关系分析判断;
C、PbO2具有强氧化性氧化锰离子为高锰酸根离子;
D、碳酸钠滴入过量盐酸溶液中会反应生成二氧化碳.
解答:
解:A、过量氨水不能溶解氢氧化铝沉淀,三氯化铝溶液中加入过量氨水反应的离子方程式:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故A错误;
B、4mol/L的NaAlO2溶液和7mol/L的HCL等体积,偏铝酸根离子和氢离子反应生成氢氧化铝沉淀,过量的氢离子溶解部分氢氧化铝沉淀,依据化学反应定量关系分析,4mol/L的NaAlO2溶液和7mol/L的HCL等体积互相均匀混合,4mol偏铝酸钠需要4mol氯化氢反应生成氢氧化铝沉淀,剩余1mol氯化氢溶解1mol氢氧化铝,反应的离子方程式:4AlO2-+7H++H2O=3Al(OH)3↓+Al3+,故B正确;
C、PbO2具有强氧化性氧化锰离子为高锰酸根离子,硝酸提供酸性环境,反应的离子方程式为5PbO2+2Mn2++4H+=5Pb2++2MnO4-+2H2O,故C正确;
D、碳酸钠滴入过量盐酸溶液中会反应生成二氧化碳,反应的离子方程式2H++CO32-=CO2↑+H2O,故D正确;
故选A.
B、4mol/L的NaAlO2溶液和7mol/L的HCL等体积,偏铝酸根离子和氢离子反应生成氢氧化铝沉淀,过量的氢离子溶解部分氢氧化铝沉淀,依据化学反应定量关系分析,4mol/L的NaAlO2溶液和7mol/L的HCL等体积互相均匀混合,4mol偏铝酸钠需要4mol氯化氢反应生成氢氧化铝沉淀,剩余1mol氯化氢溶解1mol氢氧化铝,反应的离子方程式:4AlO2-+7H++H2O=3Al(OH)3↓+Al3+,故B正确;
C、PbO2具有强氧化性氧化锰离子为高锰酸根离子,硝酸提供酸性环境,反应的离子方程式为5PbO2+2Mn2++4H+=5Pb2++2MnO4-+2H2O,故C正确;
D、碳酸钠滴入过量盐酸溶液中会反应生成二氧化碳,反应的离子方程式2H++CO32-=CO2↑+H2O,故D正确;
故选A.
点评:本题考查了离子方程式书写方法,反应实质和定量关系是解题关键,题目难度较大.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
将4gNaOH固体溶于水配成50mL溶液,其物质的量浓度为( )
| A、0.1mol/L |
| B、2mol/L |
| C、1mol/L |
| D、0.5mol/L |
下列物质都能与金属钠反应放出H2,产生H2的速率排序正确的是( )
①C2H5OH ②NaOH溶液 ③醋酸溶液.
①C2H5OH ②NaOH溶液 ③醋酸溶液.
| A、③>②>① |
| B、②>①>③ |
| C、①>②>③ |
| D、③>①>② |
关于化学键的下列叙述正确的是( )
| A、离子化合物中不可能含有共价键 |
| B、两种不同种元素原子形成的共价键一定是非极性共价键 |
| C、共价化合物中不可能含有离子键 |
| D、非金属元素形成的化合物中不可能含有离子键 |
下列叙述正确的是( )
| A、同分异构现象的广泛存在是造成有机物种类繁多的唯一原因 |
| B、乙烷在光照下与氯气反应生成的一氯代烃只有一种 |
| C、分子式为CH4O和C2H6O的物质一定互为同系物 |
| D、有机物结构中碳原子通过单键连接,剩余价键均与氢原子结合都属于烷烃 |
利用如图装置,能完成很多电化学实验.下列有关此装置的叙述中,错误的是( )
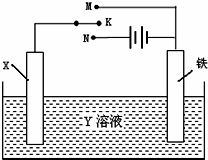

| A、若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极阴极保护法 |
| B、若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,这种方法称为外加电流阴极保护法 |
| C、若X为铜棒,Y为硫酸铜溶液,开关K置于M处时,铁电极上的电极反应式为Cu2++2e→Cu |
| D、若X为铜棒,Y为硫酸铜溶液,开关K置于N处时,溶液中各离子浓度都不会发生变化 |
在含有大量Ba2+、OH-、Cl-的溶液中还可能大量存在的离子是( )
| A、NH4+ |
| B、Ag+ |
| C、NO3- |
| D、SO42- |