题目内容
(12分)某混合溶液中可能含有的离子如下表所示:
|
可能大量含有的阳离子 |
H+、Ag+、Mg2+、Al3+、NH |
|
可能大量含有的阴离子 |
Cl-、Br-、I-、CO |
为探究其成分,进行了以下探究实验。
(1)探究一:
甲同学取一定量的混合溶液,向其中逐滴加入氢氧化钠溶液,产生沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)的关系如图所示。
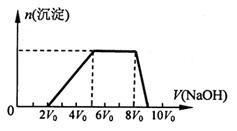
①该溶液中一定含有的阳离子是______________,其对应物质的量浓度之比为________,一定不存在的阴离子是_____________;
②请写出沉淀减少过程中发生反应的离子方程式_____________________________。
(2)探究二:
乙同学检测到该溶液中含有大量的Cl-、Br-、I-,若向1 L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
|
Cl2的体积(标准状况) |
5.6 L |
11.2 L |
22.4 L |
|
n (Cl-) |
2.5 mol |
3.0 mol |
4.0 mol |
|
n (Br-) |
3.0 mol |
2.8 mol |
1.8 mol |
|
n (I-) |
x mol |
0 |
0 |
①当通入Cl2的体积为5.6 L时,溶液中发生反应的离子方程式为_______________;
②原溶液中Cl-、Br-、I-的物质的量浓度之比为______________________。
(1)①H+、NH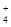 、Al3+ ; 2:3:1 ; CO
、Al3+ ; 2:3:1 ; CO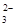 、AlO
、AlO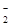
②Al(OH)3+OH ==AlO
==AlO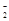 +2H2O
+2H2O
(2)Cl2+2I ==I2+2Cl
==I2+2Cl ; 10:15:4
; 10:15:4
【解析】(1)向混合液中滴加NaOH溶液,一开始无沉淀生成,说明含有H+;沉淀量最大时继续滴加NaOH溶液,不沉淀的量不变,说明含有NH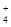 ,继续滴加,沉淀量减小直至消失,说明含有Al3+,不含有CO
,继续滴加,沉淀量减小直至消失,说明含有Al3+,不含有CO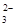 、AlO
、AlO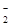 (均可与Al3+发生双水解反应),不能含有Ag+、Mg2+、Fe3+(与OH—形成的沉淀不能溶于NaOH);
(均可与Al3+发生双水解反应),不能含有Ag+、Mg2+、Fe3+(与OH—形成的沉淀不能溶于NaOH);
所涉及的反应为:H++OH-=H2O Al3++3OH-=Al(OH)3
NH4++OH-=NH3·H2O Al(OH)3+OH-=AlO2-+H2O
由题目所给数据可得出H+、NH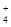 、Al3+的物质的量之比为:2:3:1
、Al3+的物质的量之比为:2:3:1
(2)当通入Cl2的体积为5.6L时,溶液中I—还有剩余,即氯气只与I-反应:Cl2+2I-=I2+2Cl-,生成0.5摩尔Cl-,Cl-初始物质的量是(2.5—0.5)mol=2 mol,Br-初始物质的量是3 mol;
当当通入Cl2的体积为11.2L时,部分溴离子(0.2mol)已被氧化:Cl2+2Br-=Br2+2Cl-,溴离子消耗氯气为 0.1 mol,故所有的I-共消耗Cl2:0.25+(0.25-0.1)=0.4mol,即原溶液中的I-是0.8 mol,则原溶液中Cl-、Br-、I-的物质的量浓度之比是10:15:4

 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案某混合溶液中可能含有的离子如下表所示:
|
可能大量含有的阳离子 |
H+、Ag+、Mg2+、Al3+、NH |
|
可能大量含有的阴离子 |
Cl-、Br-、I-、CO |
为探究其成分,进行了以下探究实验。
(1)探究一:
甲同学取一定量的混合溶液,向其中逐滴加入氢氧化钠溶液,产生沉淀的物质的量(n)与加入氢氧 化钠溶液的体积(V)的关系如图所示。

①该溶液中一定含有的阳离子是______________,其对应物质的量浓度之比为________,一定不存在的阴离子是_____________;
②请写出沉淀减少过程中发生反应的离子方程式_____________________________。
(2)探究二:
乙同学检测到该溶液中含有大量的Cl-、Br-、I-,若向1 L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如下表所示, 分析后回答下列问题:
|
Cl2的体积(标准状况) |
5.6 L |
11.2 L |
22.4 L |
|
n (Cl-) |
2.5 mol |
3.0 mol |
4.0 mol |
|
n (Br-) |
3.0 mol |
2.8 mol |
1.8 mol |
|
n (I-) |
x mol |
0 |
0 |
①当通入Cl2的体积为5.6 L时,溶液中发生反应的离子方程式为_______________;
②原溶液中Cl-、Br-、I-的物质的量浓度之比为______________________。
(12分)某混合溶液中可能含有的离子如下表所示:
|
可能大量含有的阳离子 |
H+、Ag+、Mg2+、Al3+、NH |
|
可能大量含有的阴离子 |
Cl-、Br-、I-、CO |
为探究其成分,进行了以下探究实验。
⑴探究一:
甲同学取一定量的混合溶液,向其中逐滴加入氢氧化钠溶液,产生沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)的关系如右图所示。

①该溶液中一定不存在的阳离子是______________ ,一定不存在的阴离子是__________;
含有的阳离子其对应物质的量浓度之比为__________________________________,
②请写出沉淀减少过程中发生反应的离子方程式_____________________________。
⑵探究二:
乙同学检测到该溶液中含有大量的Cl-、Br-、I-,若向1 L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
|
Cl2的体积(标准状况) |
11.2 L |
22.4 L |
28.0 L |
|
n (Cl-) |
2.5 mol |
3.5 mol |
4.0 mol |
|
n (Br-) |
3.0 mol |
2.5mol |
2.0 mol |
|
n (I-) |
x mol |
0 |
0 |
①当起始至通入Cl2的体积为22.4L时,溶液中发生反应总的离子方程式为 __________________________________________ ;
②原溶液中Cl-、Br-、I-的物质的量浓度之比为______________________。
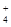 、Fe3+
、Fe3+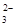 、AlO
、AlO
 、Fe3+
、Fe3+ 、AlO
、AlO
 、Fe3+
、Fe3+ 、AlO
、AlO