题目内容
(2011?台州模拟)某混合溶液中可能含有下列离子中的若干种:K+、Na+、Fe2+、Fe3+、SO42-、NO2-、CO32-,现取三份20mL该溶液进行如下实验:
(1)第一份加入足量盐酸,无任何气体产生
(2)第二份加入足量NaOH溶液,经搅拌、过滤、洗涤、灼烧,最后得到xg固体
(3)第三份滴加0.10mol?L-1酸性KMnO4溶液,消耗其体积为VmL
(4)另用洁净的铂丝蘸取该混合溶液置于浅色火焰上灼烧,发现火焰呈现黄色
根据上述实验,以下说法正确的是( )
(1)第一份加入足量盐酸,无任何气体产生
(2)第二份加入足量NaOH溶液,经搅拌、过滤、洗涤、灼烧,最后得到xg固体
(3)第三份滴加0.10mol?L-1酸性KMnO4溶液,消耗其体积为VmL
(4)另用洁净的铂丝蘸取该混合溶液置于浅色火焰上灼烧,发现火焰呈现黄色
根据上述实验,以下说法正确的是( )
分析:(1)第一份加入足量盐酸,无任何气体产生,说明溶液中不含CO32-离子,也不含NO2-离子,因NO2-+H+═HNO2,4HNO2═4NO↑+2H2O+O2↑,有气体放出,根据溶液的电中性,阴离子只有
SO42-离子,则一定存在SO42-离子.
(2)二份加入足量NaOH溶液生成沉淀,说明溶液中含有Fe2+或Fe3+离子,或二者都有,根据最后得到xg固体,可知总共含有的铁元素的物质的量;
(3)第三份滴加0.10mol?L-1酸性KMnO4溶液,消耗其体积为VmL,说明溶液中含有还原性Fe2+离子,根据消耗的高锰酸钾的物质的量可确定Fe2+离子的物质的量,并能确定是否含有Fe3+离子;
(4)另用洁净的铂丝蘸取该混合溶液置于浅色火焰上灼烧,发现火焰呈现黄色,说明含有Na+离子,但不能确定是否含有K+离子,须通过蓝色钴玻璃观察.
综上所述,溶液中一定含有Na+离子、SO42-离子,不含CO32-离子、不含NO2-离子,Fe2+或Fe3+离子至少有一种.
SO42-离子,则一定存在SO42-离子.
(2)二份加入足量NaOH溶液生成沉淀,说明溶液中含有Fe2+或Fe3+离子,或二者都有,根据最后得到xg固体,可知总共含有的铁元素的物质的量;
(3)第三份滴加0.10mol?L-1酸性KMnO4溶液,消耗其体积为VmL,说明溶液中含有还原性Fe2+离子,根据消耗的高锰酸钾的物质的量可确定Fe2+离子的物质的量,并能确定是否含有Fe3+离子;
(4)另用洁净的铂丝蘸取该混合溶液置于浅色火焰上灼烧,发现火焰呈现黄色,说明含有Na+离子,但不能确定是否含有K+离子,须通过蓝色钴玻璃观察.
综上所述,溶液中一定含有Na+离子、SO42-离子,不含CO32-离子、不含NO2-离子,Fe2+或Fe3+离子至少有一种.
解答:解:A、只有通过蓝色钴玻璃观察才能确定是否有K+离子,故A错误;
B、(1)第一份加入足量盐酸,无任何气体产生,说明溶液中不含CO32-离子,也不含NO2-离子,因NO2-+H+═HNO2,4HNO2═4NO↑+2H2O+O2↑,有气体放出,根据溶液的电中性,阴离子只有SO42-离子,则一定存在SO42-离子,故B错误;
C、足量NaOH溶液生成沉淀,说明溶液中含有Fe2+或Fe3+离子,或二者都有,根据最后得到xg固体,可知总共含有的铁元素的物质的量,滴加0.10mol?L-1酸性KMnO4溶液,消耗其体积为VmL,可以证明一定含有Fe2+离子,根据电子得失相等可得Fe2+离子的物质的量,以此来判断是否含有Fe3+离子,故C正确;
D、加入足量盐酸,无任何气体产生,说明不含NO2-离子,因NO2-+H+═HNO2,4HNO2═4NO↑+2H2O+O2↑,有气体放出,故D错误.
故选C.
B、(1)第一份加入足量盐酸,无任何气体产生,说明溶液中不含CO32-离子,也不含NO2-离子,因NO2-+H+═HNO2,4HNO2═4NO↑+2H2O+O2↑,有气体放出,根据溶液的电中性,阴离子只有SO42-离子,则一定存在SO42-离子,故B错误;
C、足量NaOH溶液生成沉淀,说明溶液中含有Fe2+或Fe3+离子,或二者都有,根据最后得到xg固体,可知总共含有的铁元素的物质的量,滴加0.10mol?L-1酸性KMnO4溶液,消耗其体积为VmL,可以证明一定含有Fe2+离子,根据电子得失相等可得Fe2+离子的物质的量,以此来判断是否含有Fe3+离子,故C正确;
D、加入足量盐酸,无任何气体产生,说明不含NO2-离子,因NO2-+H+═HNO2,4HNO2═4NO↑+2H2O+O2↑,有气体放出,故D错误.
故选C.
点评:本题考查离子鉴别题目,做题时注意从题目中找出反应的典型现象,根据物质的性质进行推断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
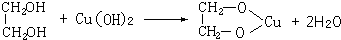
 (2011?台州模拟)下列关于有机化合物1和2的说法中正确的是( )
(2011?台州模拟)下列关于有机化合物1和2的说法中正确的是( )