题目内容
4.下列图示与对应的叙述正确的是( )| A. | 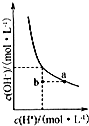 如图为在水溶液中H+和OH-的浓度变化曲线,恒温稀释可实现a→b的转化 | |
| B. |  如图为H2O2在有、无催化剂下的分解反应曲线b表示有催化剂时的反应 | |
| C. | 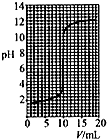 如图可表示用0.0110mol/L盐酸滴定0.0110mol/L氨水时的滴定曲线 | |
| D. | 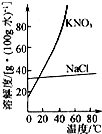 如图为NaCl中含有少量KNO3,可在较高温度下制得浓溶液再冷却结晶、过滤、干燥 |
分析 A.温度不变水溶液中离子积常数不变,H+和OH-的浓度之积为定值;
B.催化剂降低反应的活化能;
C.用0.0110mol/L盐酸滴定0.0110mol/L氨水溶液pH从大变小到恰好反应溶液显酸性;
D.硝酸钾溶解度随温度变化较大,NaCl固体中混有硝酸钾.
解答 解:A.温度不变水溶液中离子积常数不变,改变条件氢离子浓度增大则氢氧根离子浓度减小,故A错误;
B.加入催化剂,可降低反应的活化能,曲线b表示有催化剂时的反应,故B正确;
C.用0.0110mol/L盐酸滴定0.0110mol/L氨水溶液PH从大变小到恰好反应溶液显酸性,图象错误,故C错误;
D.硝酸钾溶解度随温度变化较大,NaCl固体中混有硝酸钾,应用蒸发结晶的方法除杂,故D错误.
故选B.
点评 本题考查较为综合,涉及弱电解质的电离、化学反应与能量变化、酸碱中和滴定等知识,为高考常见题型,侧重于学生的分析能力的考查,注意把握图象变化的特点,难度中等.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
4.一块表面已被氧化为Na2O的钠块10.8g,将其投入100g水中,产生H2 0.2g,则被氧化的钠是( )
| A. | 9.2 g | B. | 10.6 g | C. | 6.2 g | D. | 4.6 g |
5.将Mg、Cu组成的2.64g混合物投入适量稀硝酸中恰好反应,固体完全溶解时收集到的还原产物NO气体0.896L(标准状况),向反应后的溶液中加入2mol/L的NaOH溶液60mL时金属离子恰好沉淀完全.则形成沉淀质量为( )
| A. | 4.32 g | B. | 4.68 g | C. | 5.36 g | D. | 6.38 g |
13.下列说法正确的是( )
| A. | 钢铁在潮湿的空气中生锈是电化学腐蚀 | |
| B. | 用铂电极电解氯化钠溶液时,阳极上铂失去电子溶解,阴极上析出钠- | |
| C. | 二次电池某电极充电时作阳极,放电时作负极 | |
| D. | 原电池中电子由正极流向负极 |

 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl;②
+HCl;②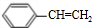 +NaCl+H2O;
+NaCl+H2O; +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$ +2NaBr;⑤2
+2NaBr;⑤2 +2H2O;
+2H2O; +H2$→_{△}^{Ni}$2
+H2$→_{△}^{Ni}$2 ;⑧n
;⑧n +nH2O.
+nH2O.
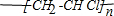
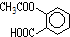 ,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.
,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.