题目内容
某恒定温度下,在一个2 L的密闭容器中充入A气体、B气体,测得其浓度2 mol/L和1 mol/L;且发生如下反应:3A(g)+2B(g)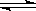 2C(?)+3D(?)ΔH =+a kJ·mol-1,已知“?”代表C、D状态未确定;反应一段时间后达到平衡,测得生成1.6 mol C,且反应前后压强比为5∶3,则下列说法中正确的是
2C(?)+3D(?)ΔH =+a kJ·mol-1,已知“?”代表C、D状态未确定;反应一段时间后达到平衡,测得生成1.6 mol C,且反应前后压强比为5∶3,则下列说法中正确的是
A.保持体积不变的情况下,向该体系中充入He气,反应速率加快,平衡正动
B.此时B的转化率为20%
C.增大该体系压强,平衡向右移动,但化学平衡常数不变
D.增加C的量,A、B转化率减小,ΔH减小
练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案
相关题目
已知反应CO(g)+2H2(g) CH3OH(g) ΔH=Q kJ·mol-1;在三个不同容积的容器中分别充入1 mol CO与2 mol H2,恒温恒容,测得平衡时CO的转化率如下表。下列说法正确的是
CH3OH(g) ΔH=Q kJ·mol-1;在三个不同容积的容器中分别充入1 mol CO与2 mol H2,恒温恒容,测得平衡时CO的转化率如下表。下列说法正确的是
温度(℃) | 容器体积 | CO转化率 | 平衡压强(p) | |
① | 200 | V1 | 50% | p1 |
② | 200 | V2 | 70% | p2 |
③ | 350 | V3 | 50% | p2 |
A.反应速率:③>①>②
B.平衡时体系压强:p1∶p2=5∶4
C.若容器体积V1>V3,则Q<0
D.若实验②中CO和H2用量均加倍,则CO转化率<70%
常温下,对下列四种溶液的叙述正确的是( )
① | ② | ③ | ④ | |
pH | 10 | 10 | 4 | 4 |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸溶液 | 盐酸 |
A.四种溶液分别加水稀释10倍,pH变化最大的是①和④
B.②、④两溶液相比,两者的kw相同
C.①、②、③中分别加入少量的醋酸铵固体后,三种溶液的pH均减小
D.①、④两溶液按一定体积比混合,所得溶液中离子浓度顺序一定为:
c(NH4+)>c(Cl-)>c(H+)> c(OH-)




 H=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,若所得混合溶液pH=2,则a:b为
H=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,若所得混合溶液pH=2,则a:b为


