题目内容
7.聚乳酸是一种新型可生物降解的高分子材料,主要用于制造可降解纤维、可降解塑料和医用材料.聚乳酸材料废弃后,先水解成乳酸(CH3-CHOH-COOH),乳酸在微生物作用下分解为CO2和H2O.乳酸的工业生产可以采用生物发酵法.淀粉$\stackrel{水解}{→}$葡萄糖$\stackrel{乳酸菌}{→}$乳酸(1)检验淀粉是否完全水解,可以选用的一种试剂是c.
a.溴水 b.银氨溶液 c.碘酒 d.碘化钾淀粉溶液
(2)乳酸分子中的官能团有羟基和羧基(写名称).
(3)乳酸分子中碳原子的杂化类型有sp2、sp3.
(4)两个乳酸分子之间可以形成环状的酯,该环状酯的结构简式是

(5)乳酸在一定条件下发生反应得到聚乳酸的化学方程式是
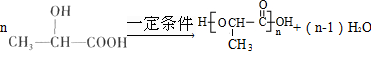 .
.
分析 (1)淀粉若完全水解,溶液中没有淀粉剩余,加入碘酒,溶液不变蓝;
(2)乳酸的结构简式为CH3-CH2OH-COOH,含有的官能团为羟基和羧基;
(3)双键C为sp2杂化,单键C为sp3杂化;
(4)根据酯化反应原理:“酸脱羟基,醇脱氢生成酯与水”解答;
(5)乳酸通过酯化反应进行的缩聚反应生成聚乳酸.
解答 解:(1)淀粉若完全水解,溶液中没有淀粉剩余,加入碘酒,溶液不变蓝,故选:c;
(2)乳酸的结构简式为CH3-CH2OH-COOH,含有的官能团为羟基和羧基,故答案为:羟基和羧基;
(3)乳酸的结构简式为CH3-CH2OH-COOH,双键C为sp2杂化,单键C为sp3杂化,故答案为:sp2、sp3;
(4)根据酯化反应原理:“酸脱羟基,醇脱氢生成酯与水”,两个乳酸分子之间可以形成环状的酯,该环状酯的结构简式是 ,
,
故答案为: ;
;
(5)乳酸在一定条件下发生反应得到聚乳酸的化学方程式是: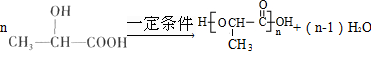 ,
,
故答案为: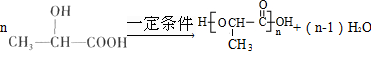 .
.
点评 本题考查乳酸的制备、合成与性质,掌握官能团的性质与转化是关键,难度中等,注意对基础知识的理解掌握.

练习册系列答案
相关题目
18.下列关于物质分类的正确组合是( )
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| A | 纯碱 | 硫酸 | 小苏打 | 氧化钙 | 干冰 |
| B | 烧碱 | 盐酸 | 食盐 | 氧化钠 | 一氧化碳 |
| C | 石灰水 | NaHSO4 | 碳酸钙 | 过氧化钠 | 二氧化碳 |
| D | NH3•H2O | HNO3 | 明矾 | 氧化铁 | SO3 |
| A. | A | B. | B | C. | C | D. | D |
15.下列有关化学用语表示正确的是( )
| A. | -CHO的电子式: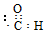 | B. | 聚丙烯的结构简式: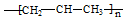 | ||
| C. | 1-丁烯的键线式: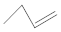 | D. | 丙烷分子的比例模型为: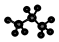 |
2.能正确表示下列化学反应的离子方程式的是( )
| A. | 氢氧化钡溶液与硫酸的反应 OH-+H+═H2O | |
| B. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+═Ca2++2H2O | |
| C. | CH3COOH溶液与NH3•H2O溶液反应:H++OH-═H2O | |
| D. | 碳酸钙溶于稀盐酸中 CaCO3+2H+═Ca2++H2O+CO2↑ |
12.下列离子方程式正确的是( )
| A. | 用NH4C1溶液溶解Mg(OH)2:Mg(OH)2+2NH4 +═Mg2十+2NH3•H2O | |
| B. | 用氨水除去NH4 C1溶液中的FeC13:Fe3++3OH-═Fe(OH)3 | |
| C. | Na2S水解:S2-+2H2O?H2S+2OH- | |
| D. | 用H2S气体作为沉淀剂除去溶液中的Cu2+:Cu2++S2-═CuS↓ |
19.在恒容的密闭容器中进行如下的可逆反应:3A(g)+B(g)?4C(g)+D(s),下列说法不能判断反应已达化学平衡状态的是( )
| A. | 反应速率v(A)=3v(B) | B. | 固体D的物质的量一定 | ||
| C. | 气体的密度不变 | D. | C的浓度不变 |
16.下列表述正确的是( )
| A. | 某离子第三层上和第二层上的电子数均为第一层的 4 倍 | |
| B. | Cl-的结构示意图: | |
| C. | 某物质的焰色反应为黄色,某物质一定为钠的化合物 | |
| D. | 14C 和 14N 的质量数相等,互称为同位素 |
17.在某温度下,可逆反应mA(g)+nB(g)?pC(g)+qD(g)平衡常数为K,下列说法正确的是( )
| A. | K越大,达到平衡时,反应进行的越完全 | |
| B. | K随反应物浓度的改变而改变 | |
| C. | K越小,达到平衡时,反应物的转化率越大 | |
| D. | K不随温度的升高而改变 |