题目内容
13.下列说法正确的是( )| A. | 常温时,NaHCO3溶液的pH值比同浓度的CH3COONa溶液小 | |
| B. | 常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c(NH4+)、c(H+)均降低 | |
| C. | 把FeCl3和FeCl2溶液分别蒸干并灼烧最后都得到Fe2O3 固体 | |
| D. | 以酚酞作指示剂,用相同浓度的盐酸滴定等体积等浓度的NaOH溶液和氨水,消耗盐酸的体积相同 |
分析 A.碳酸氢根离子的水解程度大于醋酸根离子,则相同浓度时碳酸氢钠溶液的pH大于醋酸钠;
B.稀释氨水过程中,溶液中氢氧根离子浓度减小,由于水的离子积不变,则氢离子浓度增大;
C.铁离子、亚铁离子水解分别生成氢氧化铁、氢氧化亚铁,蒸干灼烧后最终生成氧化铁;
D.酚酞的变色范围为8-10,氢氧化钠为强碱,氨水为弱碱,则pH小于8时,氨水消耗的强氧化钠溶液体积较小.
解答 解:A.常温时,由于碳酸氢钠的水解程度大于醋酸钠,则NaHCO3溶液的pH值比同浓度的CH3COONa溶液大,故A错误;
B.常温下,稀释0.1 mol/L的氨水,溶液中氢氧根离子浓度减小,但水的离子积不变,则溶液中c(H+)增大,故B错误;
C.氯化氢具有挥发性,则把FeCl3和FeCl2溶液分别蒸干并灼烧最后最终都得到Fe2O3固体,故C正确;
D.以酚酞作指示剂,当pH<8时酚酞变为无色,用相同浓度的盐酸滴定等体积等浓度的NaOH溶液和氨水,氨水为弱碱,则滴定过程中溶液变色时氨水消耗盐酸的体积较小,故D错误;
故选C.
点评 本题考查了弱电解质的电离、盐的水解原理及其影响,题目难度中等,明确弱电解质的电离平衡、盐的水解原理及其影响因素为解答关键,试题侧重考查学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
3.下列烃在光照下与氯气反应,生成两种一氯代物的有( )
| A. | 2-甲基丙烷 | B. | 2,2,3,3-四甲基丁烷 | ||
| C. | 2,2-二甲基丁烷 | D. | 2,2-二甲基丙烷 |
4.下列说法正确的是( )
| A. | 石油的分馏、裂化和煤的干馏都是化学变化 | |
| B. | 在一定条件下,苯与浓溴水、浓硝酸作用生成溴苯、硝基苯的反应都属于取代反应 | |
| C. | 尼龙、棉花、天然橡胶、ABS树脂都是由高分子化合物组成的物质 | |
| D. | 开发核能、太阳能等新能源,推广乙醇汽油,使用无磷洗涤剂都可直接降低碳排放量 |
1.草酸是二元弱酸,KHC2O4溶液呈酸性.在KHC2O4溶液中,下列表述正确的是( )
| A. | 在KHC2O4溶液中,c(K+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O42-) | |
| B. | 在KHC2O4溶液中,c(HC2O4-)+c(C2O42-)=c(K+) | |
| C. | 草酸与酸性高锰酸钾溶液反应的速率先增大后减小 | |
| D. | 草酸分子中碳元素为+3价,易发生还原反应 |
8.下列说法中正确的是( )
| A. | C60气化和I2升华克服的作用力相同 | |
| B. | 高温结构陶瓷材料Si3N4固体是分子晶体 | |
| C. | 分子晶体在水溶液中一定导电 | |
| D. | NaCl和HCl溶于水时,均破坏都是离子键 |
5.向下列溶液中通入过量CO2,最终出现浑浊的是( )
| A. | 氢氧化钙饱和溶液 | B. | 饱和的碳酸钠溶液 | ||
| C. | 硝酸钠饱和溶液 | D. | 氯化钙饱和溶液 |

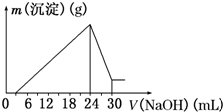 铝是现今人类生产生活中使用广泛性仅次于铁的重要金属.工业上常以“钒土矿”为原料来冶炼金属铝.已知:钒土的主要成分是Al2O3(其中含有Fe2O3、SiO2等杂质).为了检测某“钒土矿”样中Al2O3的含量,进行了如下实验过程:
铝是现今人类生产生活中使用广泛性仅次于铁的重要金属.工业上常以“钒土矿”为原料来冶炼金属铝.已知:钒土的主要成分是Al2O3(其中含有Fe2O3、SiO2等杂质).为了检测某“钒土矿”样中Al2O3的含量,进行了如下实验过程: