题目内容
由10g含有杂质的CaCO3和足量盐酸反应,产生了0.1mol CO2,推断杂质的组成不可能是( )
| A、KHCO3 |
| B、K2CO3和Na2CO3 |
| C、MgCO3和Na2CO3 |
| D、Na2CO3和NaHCO3 |
考点:有关混合物反应的计算
专题:极端假设法
分析:假设10g全部为CaCO3,与足量的盐酸反应,产生CO20.1mol,则样品中含碳量为
,碳酸钙中C的质量分数为
,故杂质中杂质中含碳平均值为12%即可(且能与酸反应生成二氧化碳).
| 12 |
| 100 |
| 12 |
| 100 |
解答:
解:假设10g全部为CaCO3,与足量的盐酸反应,产生CO20.1mol,则样品中含碳量为
,碳酸钙中C的质量分数为
,故杂质中杂质中含碳平均值为12%即可(且能与酸反应生成二氧化碳),
A.KHCO3的相对分子质量为100,样品中含碳量为
,能与盐酸反应生成二氧化碳,符合题意,故A不选;
B.K2CO3的相对分子质量为138,Na2CO3的相对分子质量为106,均能与盐酸反应生成二氧化碳,混合物中碳元素含量均小于为
,不符合题意,故B选;
C.MgCO3的相对分子质量为84,Na2CO3的相对分子质量为106,则碳的平均含量介于
~
之间,符合题意,故C不选;
D.Na2CO3的相对分子质量为106,NaHCO3的相对分子质量为84,则碳的平均含量介于
~
之间,符合题意,故D不选,
故选B.
| 12 |
| 100 |
| 12 |
| 100 |
A.KHCO3的相对分子质量为100,样品中含碳量为
| 12 |
| 100 |
B.K2CO3的相对分子质量为138,Na2CO3的相对分子质量为106,均能与盐酸反应生成二氧化碳,混合物中碳元素含量均小于为
| 12 |
| 100 |
C.MgCO3的相对分子质量为84,Na2CO3的相对分子质量为106,则碳的平均含量介于
| 12 |
| 106 |
| 12 |
| 84 |
D.Na2CO3的相对分子质量为106,NaHCO3的相对分子质量为84,则碳的平均含量介于
| 12 |
| 106 |
| 12 |
| 84 |
故选B.
点评:本题考查混合物的计算,难度中等,注意用极端假设法进行比较和判断.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案
相关题目
化学与人类生产、生活、社会可持续发展密切相关,下列说法不正确的是( )
| A、为防止富脂食品氧化变质,常在包装袋中放入生石灰 |
| B、“天宫一号”中使用的碳纤维,是一种新型无机非金属材料 |
| C、用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用 |
| D、汽车排放的尾气和冬季取暖排放颗粒污染物是形成雾霾的重要因素 |
下列物质的鉴别方法错误的是( )
| A、用酚酞溶液鉴别稀盐酸和稀氢氧化钠溶液 |
| B、用燃着的木条鉴别CO2和O2 |
| C、用稀硫酸鉴别锌片和铜片 |
| D、用加水溶解的方法即可鉴别食盐和白糖 |
下列各组有机物只用一种试剂无法鉴别的是( )
| A、乙醇、甲苯、硝基苯 |
| B、四氯化碳、己烷、己烯 |
| C、苯、甲苯、环己烷 |
| D、苯、乙醇、乙酸 |
下列物质鉴别方法中,正确的是( )
| A、用淀粉溶液鉴别NaBr、KI溶液 |
| B、用KMnO4酸性溶液鉴别CH4、C2H4气体 |
| C、用AgNO3溶液鉴别Na2SO4、NaCl溶液 |
| D、用澄清石灰水鉴别Na2CO3、NaHCO3溶液 |
用NaHCO3和KHCO3组成的混合物分别与三份同浓度的盐酸进行反应,测得数据如下:
则下列结论中不正确的是( )
| 100mL盐酸 | 100mL盐酸 | 100mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标准状况) | 2.24L | 3.36L | 3.36L |
| A、盐酸物质的量浓度为1.5mol/L |
| B、15.7g混合物与盐酸反应后有剩余 |
| C、加入9.2 g混合物时消耗HCl 0.1mol |
| D、混合物中NaHCO3和KHCO3的质量比为1:1 |
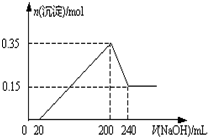 将一定质量的Mg和Al的混合物投入2.0mol/L,250mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入一定浓度的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如右图所示.回答下列问题:
将一定质量的Mg和Al的混合物投入2.0mol/L,250mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入一定浓度的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如右图所示.回答下列问题: