题目内容
下列关于相同物质的量的Na2CO3和NaHCO3的比较中,正确的是( )
| A、相同温度下,在水中的溶解度:Na2CO3<NaHCO3 |
| B、热稳定性:Na2CO3>NaHCO3 |
| C、都能与足量盐酸反应放出CO2,但产生气体的物质的量不相同 |
| D、与相同浓度的盐酸反应放出CO2的速率Na2CO3大于NaHCO3 |
考点:探究碳酸钠与碳酸氢钠的性质
专题:几种重要的金属及其化合物
分析:A.相同温度下,碳酸钠的溶解度大于碳酸氢钠;
B.碳酸氢钠加热分解生成碳酸钠、二氧化碳和水,而碳酸钠比较稳定;
C.与足量盐酸反应,二者物质的量相同,则生成二氧化碳的物质的量相等;
D.碳酸氢钠与盐酸反应的速率反应大于碳酸钠与盐酸反应速率.
B.碳酸氢钠加热分解生成碳酸钠、二氧化碳和水,而碳酸钠比较稳定;
C.与足量盐酸反应,二者物质的量相同,则生成二氧化碳的物质的量相等;
D.碳酸氢钠与盐酸反应的速率反应大于碳酸钠与盐酸反应速率.
解答:
解:A.常温下,向饱和碳酸钠溶液中通入二氧化碳气体,有碳酸氢钠晶体析出,可知常温时水溶解性:Na2CO3>NaHCO3,故A错误;
B.NaHCO3不稳定,加热易分解:2NaHCO3
Na2CO3+CO2↑+H2O,碳酸钠受热不分解,则热稳定性:Na2CO3>NaHCO3,故B正确;
C.根据碳原子守恒,二者物质的量相等时生成二氧化碳的物质的量相等,故C错误;
D.分别滴加HCl溶液,反应离子方程式为CO32-+2H+═CO2↑+H2O,HCO3-+H+═H2O+CO2↑,相同条件下NaHCO3比Na2CO3反应放出气体剧烈,故D错误;
故选B.
B.NaHCO3不稳定,加热易分解:2NaHCO3
| ||
C.根据碳原子守恒,二者物质的量相等时生成二氧化碳的物质的量相等,故C错误;
D.分别滴加HCl溶液,反应离子方程式为CO32-+2H+═CO2↑+H2O,HCO3-+H+═H2O+CO2↑,相同条件下NaHCO3比Na2CO3反应放出气体剧烈,故D错误;
故选B.
点评:本题考查了Na2CO3和NaHCO3性质,题目难度不大,注意把握Na2CO3和NaHCO3性质的异同,注重基础知识的积累,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
在标准状况下,w L氮气含有x个N2分子,则阿伏加德罗常数可表示为( )
| A、wx mol-1 | ||
B、
| ||
C、
| ||
D、
|
有机物A的相对分子质量为222,1mol A完全水解得到1mol乙酸、1mol B、1mol C,B是一种芳香族化合物,其分子式为C8H8O3,下列说法正确的是( )
| A、B中一定含有羧基和羟基 |
| B、B中一定含有羧基 |
| C、B中可能含有醛基 |
| D、B中一定不含羟基 |
随着工业的发展,大气中CO2的浓度不断增加,温室效应日益严重.为控制大气中CO2含量的增长,下列措施不切实际的是( )
| A、保护地球上的森林资源 |
| B、增加城市绿地面积 |
| C、禁止使用石油、煤碳等化石燃料 |
| D、限制CO2气体的排放 |
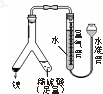 用如图所示实验装置测定某温度下气体摩尔体积,有关叙述错误的是( )
用如图所示实验装置测定某温度下气体摩尔体积,有关叙述错误的是( )| A、将水准管上提,液面高于量气管且不下降,说明装置不漏气 |
| B、可用来测定镁的相对原子质量 |
| C、读取气体体积时水准管的水面高于量气管的水面,可导致测定结果偏高 |
| D、金属镁中含有少量杂质铝,可导致测定结果偏高 |