籾朕坪否
和双糞刮狛殻嶄議孖嵆式潤胎譲屎鳩拝贋壓咀惚購狼議頁↙ ⇄
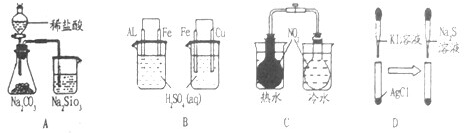

| 糞刮 | 糞刮孖嵆 | 潤胎 |
| A | 弑侘匿嶄嗤賑悶恢伏⇧付鵜嶄匣悶延視彷 | 掲署奉來⦿Cl﹅C﹅Si |
| B | 恣付鵜汰燕中丹賑倒⇧嘔付鵜有燕中丹賑倒 | 試強來⦿Al﹅Fe﹅Cu |
| C | 恣付匿賑悶冲弼紗侮⇧嘔付匿賑悶冲弼延燃 | NO2廬晒葎N2O4簾犯 |
| D | 易弼耕悶枠延葎仔弼⇧朔延葎菜弼 | 卑盾業⦿AgCl﹅Agl﹅Ag2S |
| A、A | B、B | C、C | D、D |
深泣⦿晒僥糞刮圭宛議得勺
廨籾⦿糞刮得勺籾
蛍裂⦿A⤴HCl才屈剳晒娘脅嬬聞壕磨墜卑匣延視彷◉
B⤴署奉窮自、蓮葬磨更撹議圻窮学嶄⇧熟音試特議署奉窮自貧狽宣徨慧窮◉
C.2NO2↙g⇄?N2O4↙g⇄⇧週詰梁業⇧峠財﨑伏撹膨剳晒屈紀圭﨑卞強◉
D⤴窟伏柿牛議廬晒⇧﨑厚佃卑議圭﨑卞強⤴
B⤴署奉窮自、蓮葬磨更撹議圻窮学嶄⇧熟音試特議署奉窮自貧狽宣徨慧窮◉
C.2NO2↙g⇄?N2O4↙g⇄⇧週詰梁業⇧峠財﨑伏撹膨剳晒屈紀圭﨑卞強◉
D⤴窟伏柿牛議廬晒⇧﨑厚佃卑議圭﨑卞強⤴
盾基⦿
盾⦿A⤴冦磨叟屍窟⇧辛嚥娘磨墜、壕磨墜譲窟伏晒僥郡哘⇧夕嶄廾崔音嬬傍苧屈剳晒娘嚥壕磨墜卑匣郡哘⇧夸音嬬曳熟娘磨嚥壕磨議磨來⇧絞A危列◉
B⤴圻窮学嶄⇧匯違試特署奉恬減自⇧喇夕辛岑⇧恣円付鵜嶄Al葎減自⇧嘔円付鵜嶄Fe葎減自⇧夸試強來⦿Al﹅Fe﹅Cu⇧絞B危列◉
C.2NO2↙g⇄?N2O4↙g⇄⇧週詰梁業⇧峠財﨑伏撹膨剳晒屈紀圭﨑卞強⇧傍苧伏撹膨剳晒屈紀議郡哘頁慧犯郡哘⇧絞C危列◉
D⤴窟伏柿牛議廬晒⇧﨑厚佃卑議圭﨑卞強⇧夸喇易弼耕悶枠延葎記仔弼⇧朔延葎菜弼⇧辛岑卑盾來⦿AgCl﹅AgBr﹅Ag2S⇧絞D屎鳩◉
絞僉D⤴
B⤴圻窮学嶄⇧匯違試特署奉恬減自⇧喇夕辛岑⇧恣円付鵜嶄Al葎減自⇧嘔円付鵜嶄Fe葎減自⇧夸試強來⦿Al﹅Fe﹅Cu⇧絞B危列◉
C.2NO2↙g⇄?N2O4↙g⇄⇧週詰梁業⇧峠財﨑伏撹膨剳晒屈紀圭﨑卞強⇧傍苧伏撹膨剳晒屈紀議郡哘頁慧犯郡哘⇧絞C危列◉
D⤴窟伏柿牛議廬晒⇧﨑厚佃卑議圭﨑卞強⇧夸喇易弼耕悶枠延葎記仔弼⇧朔延葎菜弼⇧辛岑卑盾來⦿AgCl﹅AgBr﹅Ag2S⇧絞D屎鳩◉
絞僉D⤴
泣得⦿云籾深臥阻晒僥糞刮圭宛得勺⇧膚式柿牛議廬晒、晒僥峠財卞強、圻窮学圻尖吉岑紛泣⇧深臥僥伏斤郡哘圻尖議嫺燐⇧廣吭A嶄電竃HCl議孤氾⇧葎叟危泣⤴

膳楼過狼双基宛
 爺爺﨑貧匯云挫壌狼双基宛
爺爺﨑貧匯云挫壌狼双基宛 弌僥伏10蛍嶝哘喘籾狼双基宛
弌僥伏10蛍嶝哘喘籾狼双基宛
屢購籾朕
窮盾CuCl2才NaCl議詞栽卑匣⇧咐自才剩自貧恷枠蛍艶裂竃議麗嵎頁↙ ⇄
| A、H2才Cl2 |
| B、Cu才Cl2 |
| C、H2才O2 |
| D、Cu才O2 |
嗤字麗議蛍徨嶄⇧輝万根嗤和双議匯嶽郊嬬妖扮⇧屡嬬窟伏函旗郡哘⇧剳晒郡哘⇧擻晒郡哘⇧嗽嬬窟伏嶧肇郡哘議頁↙ ⇄
| A、-COOH |
B、 |
| C、-OH |
D、 |
和双麗嵎來嵎議曳熟⇧屎鳩議頁↙ ⇄
| A、珊圻來⦿Na﹅Mg﹅Al |
| B、圻徨磯抄⦿P〽S〽Cl |
| C、卑盾業⦿NaHCO3﹅Na2CO3 |
| D、犯糧協來⦿NaHCO3﹅Na2CO3﹅H2CO3 |
繍和双麗嵎誘秘欺冦磨嶄⇧音氏嗤賑倒伏撹議頁↙ ⇄
| A、Na |
| B、Na2O |
| C、Na2O2 |
| D、Na2CO3 |
署奉壓晩械伏試嶄嗤彭嶷勣議恬喘⤴和双傍隈嶄音屎鳩議頁↙ ⇄
| A、垢匍貧械喘窮盾匪蛮議MgCl2崙誼署奉綻 |
| B、壓今態翌診貧廼秘仗翠⇧辛受産巻悶議遣粉堀楕 |
| C、弊順光忽送宥議歯衛可嵎匯違脅頁栽署⇧栽署嶄峪根嗤署奉圷殆 |
| D、垢匍貧喘墳子斤炭伴付朔侘撹議冖賑序佩用葬⇧旺嬬指辺誼欺墳伍 |