题目内容
设NA表示阿伏加德罗常数的值,下列有关NA 的叙述中不正确的有
A.标准状况下,20 g重水(D2O)中含有的电子数为10NA
B.乙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA
C.22.4 L的N2的共用电子对数为3NA
D.78gNa2O2固体中含有的阴离子数为NA
C
【解析】
试题分析:A.标准状况下,20 g重水(D2O)的物质的量是20g÷20g/mol=1mol,其中含有的电子数为10NA,A正确;B.乙烯和环丙烷的最简式相同,都是CH2,则组成为42 g混合气体中氢原子的物质的量是 ×2=6mol,因此氢原子个数为6NA,B正确;C.22.4 L的N2的共用电子对数不一定为3NA,氧气氮气不一定处于标准状况下,22.4L氮气的物质的量不一定是1mol,C错误;D.78gNa2O2固体的物质的量是1mol,其中含有的阴离子数为NA,D正确,答案选C。
×2=6mol,因此氢原子个数为6NA,B正确;C.22.4 L的N2的共用电子对数不一定为3NA,氧气氮气不一定处于标准状况下,22.4L氮气的物质的量不一定是1mol,C错误;D.78gNa2O2固体的物质的量是1mol,其中含有的阴离子数为NA,D正确,答案选C。
考点:考查阿伏伽德罗常数的计算

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(12分)高锰酸钾是一种典型的强氧化剂,无论在实验室还是在化工生产中都有重要的应用。如图K10?3是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。

图K10?3
(1)制备氯气选用的药品为高锰酸钾和浓盐酸,相应的离子方程式为___________________________。
(2)装置B的作用是________________________,实验进行时C中可能发生堵塞,请写出发生堵塞时B中的现象:______________________________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入____(选“a”“b”或“c”)。
a | b | c | |
I | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。当向D中缓缓通入足量氯气时,可以看到无色溶液逐渐变为红棕色,说明氯的非金属性大于溴。打开活塞,将D中的少量溶液加入E中,振荡E,观察到的现象是________________________________。该现象________(填“能”或“不能”)说明溴的非金属性强于碘。
下列有关化学用语表示不正确的是
A.氧的原子结构示意图: |
B.Na2O2的电子式: |
| C.HClO的结构式:H—O—Cl |
D.中子数为16的硫离子: S2- S2- |
不同固态物质分子1 mol,体积大小并不相同,主要原因是
| A.微粒大小不同 | B.微粒质量不同 |
| C.微粒间平均距离不同 | D.微粒间引力不同 |
 Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,
Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,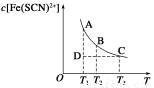
 Fe(SCN)2+(aq) ΔH>0
Fe(SCN)2+(aq) ΔH>0

