题目内容
FeCl3(aq)与KSCN(aq)混合时存在下列平衡:Fe3+(aq)+SCN-(aq)  Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,
Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,
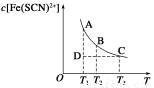
则下列说法正确的是
A.FeCl3(aq)与KSCN(aq)反应的热化学反应方程式为:Fe3+(aq)+SCN—(aq) Fe(SCN)2+(aq) ΔH>0
Fe(SCN)2+(aq) ΔH>0
B.温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1<K2
C.反应处于D点时,一定有υ正>υ逆
D.A点与B点相比,A点的c(Fe3+)大
C
【解析】
试题分析:A、根据图像可知温度越高物质的量浓度c[Fe(SCN)2+]越小,这说明升高温度平衡向逆反应方向进行,因此正方应是放热反应,即ΔH<0,A错误;B、温度为T1<T2时,升高温度平衡向逆反应方向进行,平衡常数减小,则K1>K2,B错误;C、反应处于D点时没有达到平衡状态,此时要达到平衡状态,物质的量浓度c[Fe(SCN)2+]必须增大,即反应向正反应方向进行,则一定有υ正>υ逆,C正确;D、B点温度高,平衡有利于向逆反应方向进行,所以A点与B点相比,A点的c(Fe3+)小,D错误,答案选C。
考点:考查外界条件对平衡状态的影响

练习册系列答案
相关题目
下列有关化学用语的表示正确的是
A.NH4Cl的电子式: | B.Cl-的结构示意图: |
| C.中子数为21的钾原子:4019K | D.对硝基苯酚的结构简式: |
下列化学用语不能正确表示相应粒子的是
A.HClO的电子式: |
| B.C2H6的结构简式:CH3CH3 |
| C.CO2的结构式:O=C=O |
D.O2-的结构示意图: |
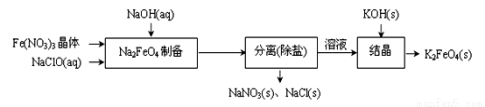
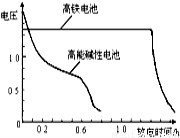

 Na2S2O3
Na2S2O3