题目内容
常温时0.1mol?L-1HA溶液的pH>1,0.1mol?L-1BOH溶液中c(OH-):c(H+)=1012,将两溶液等体积混合,以下判断正确的是( )
| A.c(H+)<c(OH-)<c(A-)<c(B+) | B.c(OH-)<c(H+)<c(B+)<c(A-) |
| C.c(H+)+c(B+)<c(A-)+c(OH-) | D.c(A-)=c(B+)>c(H+)=c(OH-) |
常温时0.1mol?L-1HA溶液的pH>1,说明HA没有完全电离,应为弱酸,
0.1mol?L-1BOH溶液中c(OH-):c(H+)=1012,
则:c(OH-)=
=
,
解之得:c(OH-)=0.1mol/L,
说明碱完全电离,为强碱,
二者反应后生成强碱弱酸盐,溶液中存在A-+H2O
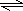
HA+OH-,呈碱性,
则有c(H+)<c(OH-)<c(A-)<c(B+),
根据溶液电中性原则,则有:c(H+)+c(B+)=c(A-)+c(OH-),
故选A.
0.1mol?L-1BOH溶液中c(OH-):c(H+)=1012,
则:c(OH-)=
| 1012 |
| c(H+) |
| 1012 | ||
|
解之得:c(OH-)=0.1mol/L,
说明碱完全电离,为强碱,
二者反应后生成强碱弱酸盐,溶液中存在A-+H2O
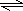
HA+OH-,呈碱性,
则有c(H+)<c(OH-)<c(A-)<c(B+),
根据溶液电中性原则,则有:c(H+)+c(B+)=c(A-)+c(OH-),
故选A.

练习册系列答案
相关题目