题目内容
12.下列有水参加的反应中,属于氧化还原反应,但水既不是氧化剂,又不是还原剂的是( )| A. | 金属钠与水反应 | B. | 氧化钠和水反应 | ||
| C. | 过氧化钠和水反应 | D. | 碳酸钠与水和二氧化碳反应 |
分析 A.Na与水反应生成NaOH和氢气;
B.氧化钠与水反应生成NaOH;
C.过氧化钠与水反应生成NaOH和氧气;
D.碳酸钠与水和二氧化碳反应,生成碳酸氢钠.
解答 解:A.Na与水反应生成NaOH和氢气,Na、H元素的化合价变化,为氧化还原反应,水中H元素化合价降低,水为氧化剂,故A不选;
B.氧化钠与水反应生成NaOH,无元素的化合价变化,为非氧化还原反应,故B不选;
C.过氧化钠与水反应生成NaOH和氧气,只有过氧化钠中O元素的化合价变化,属于氧化还原反应,但水既不是氧化剂,又不是还原剂,故C选;
D.碳酸钠与水和二氧化碳反应,生成碳酸氢钠,无元素的化合价变化,为非氧化还原反应,故D不选;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握发生的反应、反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意判断常见元素的化合价,题目难度不大.

练习册系列答案
相关题目
2.设NA为阿伏加德罗常数的数值.下列说法正确的是( )
| A. | 1 mol甲苯含有6NA个C-H键 | |
| B. | 标准状况下,22.4 L氨水含有NA个NH3分子 | |
| C. | 18 g H2O含有10NA个质子 | |
| D. | 56 g铁片投入足量浓H2SO4中生成NA个SO2分子 |
3.用NA表示阿伏加德罗常数的值.下列说法中正确的是( )
| A. | 0.5 mol•L-1NaCl溶液中Na+数目为0.5 NA | |
| B. | 2 g氢气中含有的原子数为NA | |
| C. | 3.01×1023个氮气分子中含有的原子数为2NA | |
| D. | 在标准状况下2.24 L氨气(NH3)所含分子数为0.1 NA |
20.据报道,在西藏冻土的一定深度下,发现了储量巨大的“可燃冰”,它主要是甲烷和水形成的化合物(CH4•nH2O).
(1)在常温常压下,“可燃冰”会发生分解反应,其化学方程式是CH4•nH2O=CH4↑+nH2O.
(2)甲烷可制成合成气(CO、H2),再制成甲醇(CH3OH),代替日益供应紧张的燃油.
①在101KPa时,1.6g CH4(g)与H2O(g)反应生成CO、H2,吸热20.64kJ.则甲烷与H2O(g)反应的热化学方程式CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.4 kJ•mol-1.
②CH4不完全燃烧也可制得合成气:CH4(g)+$\frac{1}{2}$O2(g)═CO(g)+2H2(g)△H=-35.4kJ•mol-1,则从原料选择和能源利用角度,比较方法①和②,合成甲醇的适宜方法为②(填序号).
(3)利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇(CH3OH),发生的主要反应如下:CO和甲醇的结构式如图1所示:
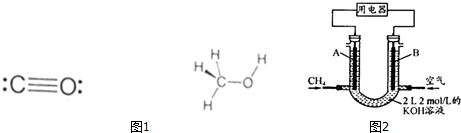
①CO(g)+2H2(g)=CH3OH(g)△H1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)=CO(g)+H2O(g)△H3
回答下列问题:
已知反应①中相关的化学键键能数据如下:
由此计算△H1=-99kJ•mol-1,已知△H2=-58kJ•mol-1,则△H3=+41kJ•mol-1.
(4)可燃冰中CH4的其它用途是能源和燃料,将CH4设计成燃料电池,其利用率更高,装置示意如图2(A、B为多孔性碳棒).持续通入甲烷,在标准状况下,消耗甲烷体积VL.当44.8L<V≤89.6L时,负极电极反应为CH4-8e-+9CO32-+3H2O=10HCO3-.
(1)在常温常压下,“可燃冰”会发生分解反应,其化学方程式是CH4•nH2O=CH4↑+nH2O.
(2)甲烷可制成合成气(CO、H2),再制成甲醇(CH3OH),代替日益供应紧张的燃油.
①在101KPa时,1.6g CH4(g)与H2O(g)反应生成CO、H2,吸热20.64kJ.则甲烷与H2O(g)反应的热化学方程式CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.4 kJ•mol-1.
②CH4不完全燃烧也可制得合成气:CH4(g)+$\frac{1}{2}$O2(g)═CO(g)+2H2(g)△H=-35.4kJ•mol-1,则从原料选择和能源利用角度,比较方法①和②,合成甲醇的适宜方法为②(填序号).
(3)利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇(CH3OH),发生的主要反应如下:CO和甲醇的结构式如图1所示:

①CO(g)+2H2(g)=CH3OH(g)△H1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)=CO(g)+H2O(g)△H3
回答下列问题:
已知反应①中相关的化学键键能数据如下:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 1076 | 465 | 413 |
(4)可燃冰中CH4的其它用途是能源和燃料,将CH4设计成燃料电池,其利用率更高,装置示意如图2(A、B为多孔性碳棒).持续通入甲烷,在标准状况下,消耗甲烷体积VL.当44.8L<V≤89.6L时,负极电极反应为CH4-8e-+9CO32-+3H2O=10HCO3-.
7.设NA表示阿伏加德罗常数的值,下列有关说法正确的是( )
| A. | 在常温常压下,11.2LO2含有的分子数为0.5NA | |
| B. | 71gCl2所含原子数为2NA | |
| C. | 标准状况下,22.4LH2O含有的分子数为1NA | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA |
17.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 25℃,1.01×l05Pa,46gNO2中含有的分子数等于NA | |
| B. | 7.8gNa2O2含有的阴离子数目为0.2NA | |
| C. | 2.0g重水(D2O)中含有的质子数和中子数均为NA | |
| D. | 标况下,1.12LC12溶于水,转移0.05NA电子 |
4.已知在3.2g某气体中所含的分子数目约为3.01×1022,此气体的摩尔质量为( )
| A. | 32g | B. | 32g/mol | C. | 64 mol | D. | 64g/mol |
1.生活中常常涉及到一些有机化合物的知识.下列叙述中正确的是( )
| A. | 将米饭在嘴中多加咀嚼就会变甜 | |
| B. | 羊毛和棉花的主要成分都是纤维素 | |
| C. | 为提高加酶洗衣粉的去污能力,应使用热水进行洗涤 | |
| D. | 未成熟的苹果遇碘水会变蓝,是因为其中含有淀粉 |
18.某羧酸酯的分子式为C18H26O5,1mol该酯完全水解可得到2mol乙酸和1mol醇,该醇的分子式为( )
| A. | C14H18O5 | B. | C14H22O3 | C. | C14H22O5 | D. | C14H10O5 |