题目内容
下列有关化学反应的说法正确的是( )
| A、在氧化还原反应中,阴离子只能发生氧化反应 |
| B、碳酸钠溶液显碱性,碳酸钠是一种碱 |
| C、有些吸热反应不需要加热也能进行 |
| D、1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
考点:氧化还原反应,吸热反应和放热反应,燃烧热
专题:
分析:A.阴离子可能被氧化,也可能被还原;
B.碳酸钠为盐类物质;
C.反应中能量变化与反应条件无关;
D.1mol可燃物燃烧生成稳定氧化物放出的热量是燃烧热.
B.碳酸钠为盐类物质;
C.反应中能量变化与反应条件无关;
D.1mol可燃物燃烧生成稳定氧化物放出的热量是燃烧热.
解答:
解:A.阴离子可能被氧化,也可能被还原,如亚硫酸根离子与氯气反应时阴离子被氧化,亚硫酸根离子与硫化氢反应时阴离子被还原,故A错误;
B.碳酸钠为盐类物质,碳酸根离子水解使溶液显碱性,故B错误;
C.反应中能量变化与反应条件无关,有些吸热反应不需要加热也能进行,如八水合氯化铵和氢氧化钡的反应,故C正确;
D.1mol可燃物燃烧生成稳定氧化物放出的热量是燃烧热,而1mol甲烷燃烧生成气态水不是稳定氧化物,应为液态水和二氧化碳所放出的热量是甲烷的燃烧热,故D错误;
故选C.
B.碳酸钠为盐类物质,碳酸根离子水解使溶液显碱性,故B错误;
C.反应中能量变化与反应条件无关,有些吸热反应不需要加热也能进行,如八水合氯化铵和氢氧化钡的反应,故C正确;
D.1mol可燃物燃烧生成稳定氧化物放出的热量是燃烧热,而1mol甲烷燃烧生成气态水不是稳定氧化物,应为液态水和二氧化碳所放出的热量是甲烷的燃烧热,故D错误;
故选C.
点评:本题考查较综合,为高频考点,涉及氧化还原反应、盐类水解、反应中能量变化及燃烧热等,侧重高考高频考点的考查,注意AC利用实例分析,题目难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
下列物质的分子中既有σ键又有π键还有离子键的是( )
①CO2 ②CaC2(电石) ③N2 ④Na2O2 ⑤C2H4 ⑥C2H2.
①CO2 ②CaC2(电石) ③N2 ④Na2O2 ⑤C2H4 ⑥C2H2.
| A、只有①②③ | B、只有①③⑤⑥ |
| C、只有①②⑤ | D、只有② |
室温下,甲、乙两烧杯均盛有5mL pH=3的某一元酸溶液,向乙烧杯中加水稀释至pH=4.关于甲、乙两烧杯中溶液的描述正确的是( )
| A、溶液的体积:10V甲≤V乙 |
| B、水电离出的OH-浓度:10c(OH-)甲≤c(OH-)乙 |
| C、若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙 |
| D、若分别与5mL pH=11的NaOH溶液反应,所得溶液的pH:甲≤乙 |
共价键、离子键、配位键和范德华力是粒子之间的四种作用力.现有下列晶体:①Na2O2②SiO2③[Cu(NH3 )4]Cl2④NH4Cl ⑤NaCl ⑥AlCl3,其中含有三种作用力的是( )
| A、只有①②③ |
| B、只有①②③⑥ |
| C、只有③④⑥ |
| D、只有③④ |
卤素间形成的化合物如“IF5、BrCl、IBr”等称为卤素互化物,化学性质与卤素单质类似,则下列关于卤素互化物的性质的描述及发生的相关反应不正确的是( )
| A、IF5+3H2O═HIO3+5HF |
| B、3IBr+2Fe═FeI3+FeBr3 |
| C、BrCl的氧化性强于I2 |
| D、IBr可以与NaOH溶液反应生成2种盐 |
 A、B、C三种物质的物质的量随时间变化的关系图.
A、B、C三种物质的物质的量随时间变化的关系图.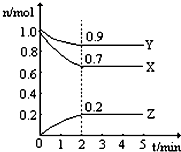 某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线,如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线,如图所示.根据图中数据,试填写下列空白: