题目内容
如图所示的装置中,A是氯气发生装置,C、D为气体净化装置(C中装有饱和食盐水;D 中装有浓硫酸),E是硬质玻璃管装有细铁丝网,F为干燥的空广口瓶,烧杯G中装有氢氧化钠溶液.

试回答:
(1)实验室制氯气的化学方程式: ;
(2)C装置的作用是 ;D装置的作用是 ;E中发生化学反应的方程式为: .
(3)烧杯G中装有氢氧化钠溶液的作用是 ;.

试回答:
(1)实验室制氯气的化学方程式:
(2)C装置的作用是
(3)烧杯G中装有氢氧化钠溶液的作用是
考点:实验装置综合,氯气的实验室制法
专题:实验题
分析:在加热条件下,二氧化锰和浓盐酸反应生成氯气、氯化锰和水;浓盐酸具有挥发性,导致制取的氯气中含有HCl,HCl极易溶于水,饱和食盐水中含有氯离子抑制氯气溶解,所以用饱和食盐水吸收氯化氢;D中含有浓硫酸,浓硫酸具有吸水性,能作干燥剂;在加热条件下,铁丝和氯气发生氧化还原反应生成氯化铁;氯气密度大于空气且常温下和空气不反应,可以采用向上排空气法收集氯气;氯气有毒不能直接排空,可以用碱性物质吸收氯气.
解答:
解:在加热条件下,二氧化锰和浓盐酸反应生成氯气、氯化锰和水;浓盐酸具有挥发性,导致制取的氯气中含有HCl,HCl极易溶于水,饱和食盐水中含有氯离子抑制氯气溶解,所以用饱和食盐水吸收氯化氢;D中含有浓硫酸,浓硫酸具有吸水性,能作干燥剂;在加热条件下,铁丝和氯气发生氧化还原反应生成氯化铁;氯气密度大于空气且常温下和空气不反应,可以采用向上排空气法收集氯气;氯气有毒不能直接排空,可以用碱性物质吸收氯气,
(1)加热条件下,二氧化锰和浓盐酸反应生成氯气、氯化锰和水,反应方程式为:MnO2+4 HCl(浓)
MnCl2+Cl2↑+2 H2O,故答案为:MnO2+4 HCl(浓)
MnCl2+Cl2↑+2 H2O;
(2)浓盐酸具有挥发性,导致制取的氯气中含有HCl,HCl极易溶于水,饱和食盐水中含有氯离子抑制氯气溶解,所以用饱和食盐水吸收氯化氢;浓硫酸具有吸水性而干燥氯气;在加热条件下,铁丝和氯气发生氧化还原反应生成氯化铁,反应方程式为,故答案为:除去氯气中混有的氯化氢;干燥氯气;2 Fe+3 Cl2
2 FeCl3;(3)氯气有毒不能直接排空,氯气和碱性物质反应生成无毒物质,所以E装置的作用是吸收多余的氯气,反应方程式为Cl2+2 NaOH=NaCl+NaClO+H2O,故答案为:吸收多余的氯气.
(1)加热条件下,二氧化锰和浓盐酸反应生成氯气、氯化锰和水,反应方程式为:MnO2+4 HCl(浓)
| ||
| ||
(2)浓盐酸具有挥发性,导致制取的氯气中含有HCl,HCl极易溶于水,饱和食盐水中含有氯离子抑制氯气溶解,所以用饱和食盐水吸收氯化氢;浓硫酸具有吸水性而干燥氯气;在加热条件下,铁丝和氯气发生氧化还原反应生成氯化铁,反应方程式为,故答案为:除去氯气中混有的氯化氢;干燥氯气;2 Fe+3 Cl2
| ||
点评:本题考查了氯气的实验室制取,明确反应原理是解本题关键,根据物质的性质再结合物质之间的反应来分析解答,知道仪器的连接顺序,明确每个装置中发生的化学反应,题目难度不大.

练习册系列答案
相关题目
下列文字表述与反应方程式对应不正确的是( )
| A、氯气和水反应:Cl2+H2O═2H++Cl-+ClO- | ||
| B、用醋酸除去水垢:CaCO3+2CH3COOH═Ca2++2CH3COO--+H2O+CO2↑ | ||
| C、将丙烯通入溴水中:CH3-CH═CH2+Br2→CH3CHBrCH2Br | ||
D、甲烷与氧气反应:CH4+2O2
|
能充分说明在恒温恒容下的密闭容器中,N2(g)+O2(g)?2NO(g)已达到化学平衡状态的是( )
| A、N2、O2和NO的物质的量浓度相等 |
| B、反应体系中的压强不随时间变化 |
| C、N2、O2、NO三种物质同时存在 |
| D、单位时间内生成1mol N2 同时消耗1mol O2 |




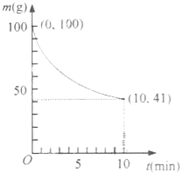 镍具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料.羰基法提纯粗镍涉及的两步反应依次为:
镍具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料.羰基法提纯粗镍涉及的两步反应依次为: